准确称取6克铝土矿样品(含Al2O3、Fe2O3、SiO2)加入100mL硫酸溶液,充分反应后,向滤液中加入10mol/L NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,求所用硫酸溶液的物质的量浓度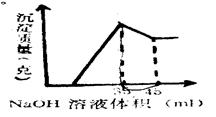
| A.1.75 mol/L | B.3.5 mol/L | C.2.25 mol/L | D.无法计算 |
有t℃的a g KCl不饱和溶液,其质量分数为w1,采取措施后使其变为b g饱和溶液,其溶质质量分数为w2,下列说法正确的是
| A.a一定小于或等于b | B.aw1一定等于b w2 |
| C.t℃时KCl溶解度一定大于100w1 | D.w1一定大于w2 |
设nA为阿伏加德罗常数的值,下列说法正确的是
| A.1 mol·L-1的K2SO4溶液中有2nA个K+ |
| B.1 mol Cl2与足量铁反应,转移2nA个电子 |
| C.标准状况下,22.4L氨气溶于水,此溶液中含有nA个NH3分子 |
| D.所含溶质为63g的浓硝酸与足量的铜反应,生成的气体分子数为0.5nA |
下列相关表达正确的是
| A.亚硫酸的电离方程式:H2SO3=2H++SO2- 3 |
| B.中子数为18的氯原子的原子符号:18 17Cl |
| C.(CH3)2CHCH2CH2OH的名称:3-甲基-1-丁醇 |
D.HOCH2COOH缩聚产物的结构简式: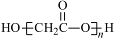 |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.标准状况下,22.4 L SO3中含有的氧原子数为3NA |
| B.标准状况下,22.4 L Cl2与足量的稀NaOH 溶液反应,转移电子总数为2NA |
| C.1 mol N5+共有34 NA核外电子 |
| D.0.5 mol CCl4中含有共价键数目为4NA |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,2.24L苯中含有的C-H键的数目为0.6NA |
| B.标准状况下,由H2O2制得4.48LO2转移的电子数目为0.8NA |
| C.14 g由乙烯与环丙烷组成的混合气体含有的碳原子数目为NA |
| D.常温下,1 L pH=2的H2SO4溶液中含有的H+数目为0.02NA |
NA表示阿伏伽德罗常数的值,下列说法正确的是
| A.在标准状况下,11.2L NH3含有5NA个质子 |
| B.Na2O2与CO2反应产生1molO2时,转移电子数为4NA |
| C.SO2、CO2、NO、NO2都是大气污染物,实验中都必须进行尾气吸收 |
| D.明矾和漂白粉常用于自来水的净化或杀菌消毒,两者的作用原理相同 |
设NA为阿伏加德罗常数的数值,下列说法中正确的是
| A.1mol Fe2+与足量的H2O2溶液反应,转移2nA个电子 |
| B.标准状况下,22.4L NO2气体中含有NA个O2分子 |
| C.常温常压下,15g HCHO含有2NA对共用电子对 |
| D.1L 0.1mol?L-1的醋酸溶液中有NA个CH3COO- |
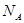 表示阿伏加德罗常数,下列叙述中正确的是
表示阿伏加德罗常数,下列叙述中正确的是 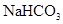 晶体中阳离子和阴离子总数为0.03NA
晶体中阳离子和阴离子总数为0.03NA