题目内容
有t℃的a g KCl不饱和溶液,其质量分数为w1,采取措施后使其变为b g饱和溶液,其溶质质量分数为w2,下列说法正确的是
| A.a一定小于或等于b | B.aw1一定等于b w2 |
| C.t℃时KCl溶解度一定大于100w1 | D.w1一定大于w2 |
C
解析试题分析:A. KCl的溶解度受温度的影响变化较大,若是温度不变,向溶液中加入KCl使其变为饱和溶液,则a<b;若是降低温度使溶液恰好变为饱和溶液,则a=b;若是还析出了晶体,则a>b。错误。B.在变化的过程中若是未加入溶质或析出晶体,则aw1="b" w2;若是加入了KCl或析出晶体KCl,则二者不相等。错误。C.在t℃时a g KCl不饱和溶液,其质量分数为w1,,若变为饱和溶液,则就要加入溶质,因此溶液的质量分数就大于w1,所以KCl溶解度一定大于100w1 。正确。D.若为同一温度下的溶液,或高于t℃的溶液则w2一定大于w1;若是温度低于t℃,则w1一定大于w2。错误。
考点:考查饱和溶液与不饱和溶液的质量分数、溶解度的关系的知识。

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
溶于水时,下列物质或微粒对水的电离平衡不产生影响的是
A.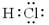 | B.13Al3+ | C.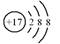 | D.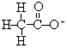 |
N0代表阿伏伽德罗常数的值。已知C3H6和C6H12的混合物的质量为m g,则该混合物
| A.所含共用电子对数目为 3m N0/14 | B.所含原子总数为m N0 /14 |
| C.燃烧时消耗的O2一定是33.6m/14 L | D.所含碳氢键数目为m N0/7 |
NA表示阿伏加德罗常数的值,下列叙述中不正确的是
| A.Fe与标准状况下2.24LCl2恰好完全反应,转移电子数目为0.2NA |
| B.0.5molNa2O2和0.5molNa2O组成的混合物中,含阴离子数目为1.5NA |
| C.17gNH3分子中含有的共用电子对数为3NA |
| D.1.7gOH—所含电子总数为NA |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,2.24L苯中含有的C-H键的数目为0.6NA |
| B.标准状况下,由H2O2制得4.48LO2转移的电子数目为0.8NA |
| C.14 g由乙烯与环丙烷组成的混合气体含有的碳原子数目为NA |
| D.常温下,1 L pH=2的H2SO4溶液中含有的H+数目为0.02NA |
用NA表示阿伏加德罗常数的值。下列说法正确的是
| A.2.24LCO2中含有的原子数为0.3NA |
| B.1.8g NH4+离子中含有的质子数为NA |
| C.C60和石墨的混合物共1.8g,含碳原子数目为0.15NA |
| D.0.5mol/LNaOH溶液中,含Na+离子数目为0.5NA |
NA为阿伏加德罗常数的值。下列叙述正确的是
| A.1.0 L 1.0 mol·L-1的NaClO水溶液中含有的氧原子数为NA |
| B.25 ℃时1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA |
| C.2.24 L的2H35Cl分子中的中子数是1.9NA |
| D.某密闭容器中盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,形成N—H键的数目为0.6NA |
下列电子式书写正确的是 ( )
A.氮气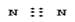 | B.二氧化碳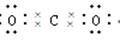 |
C.水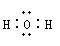 | D.氯化铵 |
下列有关概念间关系的说法正确的是
| A.碱性氧化物一定是金属氧化物 |
| B.氧化剂在化学反应中一定被氧化 |
| C.酸性氧化物一定是非金属氧化物 |
| D.摩尔质量相同的物质其摩尔体积一定相同 |