某探究小组利用丙酮的溴代反应(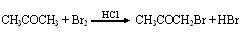 )来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
)来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
|
实验 序号 |
初始浓度c/mol·l-1 |
溴颜色消失所需时间t/s |
||
|
CH3COCH3 |
HCl |
Br2 |
||
|
① |
0.80 |
0.20 |
0.0010 |
290 |
|
② |
1.60 |
0.20 |
0.0010 |
145 |
|
③ |
0.80 |
0.40 |
0.0010 |
145 |
|
④ |
0.80 |
0.20 |
0.0020 |
580 |
分析实验数据所得出的结论不正确的是( )
A.增大c(CH3COCH3),υ(Br2)增大 B.实验②和③的υ(Br2)相等
C.增大c(HCl),υ(Br2)增大 D.增大c(Br2),υ(Br2)增大
已知A(g)+B(g)  C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
|
|温度/ ℃ |
700 |
900 |
830 |
1000 |
1200 |
|
平衡常数 |
1.7 |
1.1 |
1.0 |
0.6 |
0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。,则6s时c(A)= mol·L-1, C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为 ;
(3)判断该反应是否达到平衡的依据为 (填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c. c(A)不随时问改变 d.单位时间里生成c和D的物质的量相等
(4)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为
。
A(g)+B(g)的平衡常数的值为
。
盐酸或硫酸和氢氧化钠溶液的中和反应没有明显的现象。某学习兴趣小组的同学为了证明氢氧化钠溶液与盐酸或硫酸发生了反应,从中和反应的热效应出发,设计了下面几种实验方案。请回答有关问题。
(1)方案一:如图1装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上。开始时使右端U形管两端红墨水相平。实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是_________ ,原因是___________。
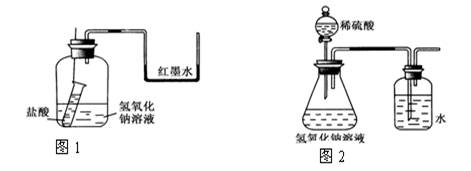
(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生。如果氢氧化钠溶液与盐酸混合前后有温度的变化,则证明发生了化学反应。该小组同学将不同浓度的氢氧化钠溶液和盐酸各10 mL混合,用温度计测量反应前后温度的变化,测得的部分数据如下表:
|
编号 |
盐酸 |
氢氧化钠 |
△t/℃ |
|
1 |
0.1 mol·L-1 |
0.05 mol·L-1 |
3.5 |
|
2 |
0.1 mol·L-1 |
0.1 mol·L-1 |
x |
|
3 |
0.2 mol·L-1 |
0.2 mol·L-1 |
14 |
则x=____________。
(3)方案三:该小组还设计了如图2示装置来证明氢氧化钠溶液确实与稀硫酸发生了反应。他们认为若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,从而证明发生了反应。
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可能是______________
②从原理上讲,该实验设计的不合理之处为__________________________________。
请你在此实验装置的基础上提出修改方案__________________________________。
 Ag2O(s)+SO3(g) ,2 SO3(g)
Ag2O(s)+SO3(g) ,2 SO3(g)
 Cl2(g) + CO(g) △H = + 108 KJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10 min到14
min的COCl2浓度变化曲线未画出):
Cl2(g) + CO(g) △H = + 108 KJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10 min到14
min的COCl2浓度变化曲线未画出):
