固体碘化铵置于密闭容器中,加热至一定温度后恒温;容器中发生反应:
①NH4I(s)?NH3(g)+HI(g)
②2HI(g)?H2(g)+I2(g),测得平衡时c(H2)=0.5mol/L,反应①的平衡常数为20,
则下列结论正确的是( )
①NH4I(s)?NH3(g)+HI(g)
②2HI(g)?H2(g)+I2(g),测得平衡时c(H2)=0.5mol/L,反应①的平衡常数为20,
则下列结论正确的是( )
| A、固体碘化铵一定完全分解 | B、当固体碘化铵物质的量增大一倍,则在相同条件下,容器内压强也增大一倍 | C、平衡时HI分解率为40% | D、平衡时C(NH3)=5mol/L |
向体积为2L的密闭容器中充入2mol SO2和1mol O2,测得起始容器压强为p,一定条件下发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-196kJ?mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2mol SO3,则下列说法正确的是( )
| A、充入2 mol SO3后,SO2的物质的量增大 | B、第一次反应达到平衡时共放出热量176.4 kJ | C、充入2 mol SO3达到新平衡时,容器内的压强为1.4p | D、降低容器的温度可使新平衡时各物质的体积分数与第一次平衡时相同 |
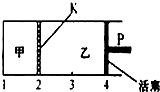 已知可逆反应:A(s)+2B(g)═C(g)+D(g)△H<0.在一定温度下将1mol A和2molB加入如图所示甲容器中,将2molC和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,在恒温下使两容器内反应均达到平衡状态(如图所示,隔板K不能移动).下列说法正确的是( )
已知可逆反应:A(s)+2B(g)═C(g)+D(g)△H<0.在一定温度下将1mol A和2molB加入如图所示甲容器中,将2molC和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,在恒温下使两容器内反应均达到平衡状态(如图所示,隔板K不能移动).下列说法正确的是( )| A、保持乙中压强不变,升高温度,达到新的平衡后,乙中平均相对分子质量增大 | B、保持温度和乙中压强不变,向乙中再加入2 mol D,达到新平衡后,一定有c(B)乙>c(B)甲 | C、若该温度下反应的K=1,则甲中B和乙中C的转化率均为66.7% | D、保持温度和活塞位置不变,甲中再加入1 mol A和2mol B,达到新的平衡后,c(B)甲=2c(B)乙 |
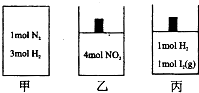 如图所示的甲、乙、丙三个绝热容器中分别发生的反应为:
如图所示的甲、乙、丙三个绝热容器中分别发生的反应为:甲:N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol
乙:2NO2(g)?N2O4
丙:H2(g)+I2(g)?2HI(g)
则下列有关说法不正确的是( )
| A、若甲的体积为2L,经过10秒后反应达到平衡状态,放出热量为55.44U,则H2的反应速率是0.09mol/(L?s) | B、若甲、乙中反应达到平衡时的体积相同,则两容器中所含物质的量可能相同 | C、若乙、丙中反应达到平衡时的体积、压强均相同,则乙中NO2的转化率为50% | D、若甲、乙、丙中反应均达到平衡状态时,则甲中物质的平均相对分子质量不变,乙中物质的颜色不变,丙中的温度不变 |
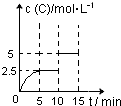 一定温度下有可逆反应:A(g)+2B(g)?2C(g)+D(g).现将4molA和8molB加入一体积为2L的密闭容器中,反应至10min时,改变某一条件,C的物质的量浓度随时间变化关系如图所示.下列有关说法正确的是( )
一定温度下有可逆反应:A(g)+2B(g)?2C(g)+D(g).现将4molA和8molB加入一体积为2L的密闭容器中,反应至10min时,改变某一条件,C的物质的量浓度随时间变化关系如图所示.下列有关说法正确的是( )| A、在0~5min内,正反应速率逐渐增大 | B、反应从起始至8min时,A的转化率为50% | C、5min时的平衡常数与10min时的平衡常数不等 | D、第15min时,B的体积分数为25% |
在恒温恒容的甲、乙、丙3个密闭容器中,按不同方式投入反应物,发生反应:
3A(g)+B(g)?xC(g)△H=-Q kJ?mol-1(Q>0)
反应物的投入量、测得反应达平衡时的有关数据如下表:
下列说法正确的是( )
3A(g)+B(g)?xC(g)△H=-Q kJ?mol-1(Q>0)
反应物的投入量、测得反应达平衡时的有关数据如下表:
| 容器 | 甲 | 乙 | 丙 |
| 反应物的投入量 | 3molA、2molB | 6molA、4molB | nAmolA、nB molB、nC molC |
| C的体积分数 | w1 | w2 | w3 |
| 反应物的转化率 | α1 | α2 | α3 |
| 反应的能量变化 | Q1 | Q2 | Q3 |
| A、若w2=2w1,则x=4 |
| B、若α1=α2,则x>4 |
| C、不论x为何值,总有Q2>Q1 |
| D、若w1=w3且满足3nC+8nA=12nB时,可判断x=4 |
| X | Y | W | |
| n(起始状态)/mol | 2 | 1 | 0 |
| n(平衡状态)/mol | 1 | 0.5 | 1.5 |
| A、升高温度,若W的体积分数减小,则此反应△H>0 |
| B、该温度下,此反应的平衡常数K=6.75 |
| C、增大压强,正、逆反应速率均增大,平衡向正反应方向移动 |
| D、该温度下,再向该容器中加入1.5mol W,达到新平衡时,c(X)=0.75mol?L-1 |
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2(g)+H2(g)
反应过程中测定的部分数据见下表(表中t2>t1),下列说法中正确的是( )
反应过程中测定的部分数据见下表(表中t2>t1),下列说法中正确的是( )
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A、反应在t1 min内的平均速率为v(CO2)=
| ||
| B、到t1 min时,反应未达平衡状态 | ||
| C、保持700℃不变,向平衡体系中再通入0.60molCO和0.30 molH20,达到新平衡时与原平 衡相比,C0转化率增大,H2的体积分数增大 | ||
| D、温度升至800℃时,上述反应的平衡常数为0.64,则正反应为放热反应 |
将a L NH3通入某恒温恒压的密闭容器中,在一定条件下让其分解,达到平衡后气体体积增大到b L(气体体积在相同条件下测定),下列说法中正确的是( )
A、平衡后氨气的分解率为
| ||
B、平衡混合气体中H2的体积分数为
| ||
C、反应前后气体的密度比为
| ||
D、平衡后气体的平均摩尔质量为
|