为了减少汽车尾气对大气造成的污染,目前市场上推出了使用乙醇汽油(在汽油中加入适量乙醇)的汽车.下列叙述错误的是( )
| A、汽车使用乙醇汽油可以减少有害气体的排放 | B、乙醇汽油是一种化合物 | C、乙醇充分燃烧生成CO2和H2O | D、用粮食发酵可制得乙醇 |
以高粱、玉米等植物的种子为原料,经发酵、蒸馏得到一种可以缓解石油危机的物质,这种物质是( )
| A、酒精 | B、氢气 | C、木炭 | D、一氧化碳 |
化学已渗透到人类生活的各个方面,下列说法不正确的是( )
| A、交警检查司机是否酒后驾车的原理中体现了乙醇的氧化性 | B、硅胶多孔,吸附水分能力强,常用作袋装食品、瓶装药品的干燥剂 | C、在入海口的钢铁闸门上装一定数量的锌块可防止闸门被腐蚀 | D、以石油、煤和天然气为原料通过聚合反应可以获得用途广泛的高分子合成材料 |
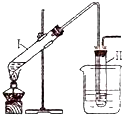 实验室用如图所示的装置制取溴乙烷.在试管Ⅰ中依次加入2mL蒸馏水、4mL浓硫酸、2mL95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水.加热试管Ⅰ至微沸状态数分钟后,冷却.已知:通常情况下,溴乙烷呈液态,其密度比水大且不溶于水.试回答下列问题:
实验室用如图所示的装置制取溴乙烷.在试管Ⅰ中依次加入2mL蒸馏水、4mL浓硫酸、2mL95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水.加热试管Ⅰ至微沸状态数分钟后,冷却.已知:通常情况下,溴乙烷呈液态,其密度比水大且不溶于水.试回答下列问题:(1)试管Ⅰ中硫酸和溴化钠加热反应生成氢溴酸.写出氢溴酸与乙醇在加热时反应的化学方程式
(2)在反应发生后试管II中可观察到的现象是
(3)溴乙烷为无色油状液体.若试管II中获得的有机物呈棕黄色,除去其中的杂质应选用的试剂是
A.CCl4 B.NaOH溶液 C.Na2SO3溶液
利用上述试剂充分洗涤后,分离混合物的操作是
(4)设计实验证明有机物溴乙烷中含有溴元素.完成以下实验报告:
| 实验步骤 | 实验操作 | 预期现象和结论 | ① | 取少量除杂后的溴乙烷于试管中, |
② | 取①中反应后的上层清液少量于另一支试管中, |
如图是实验室制备1,2-二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略).
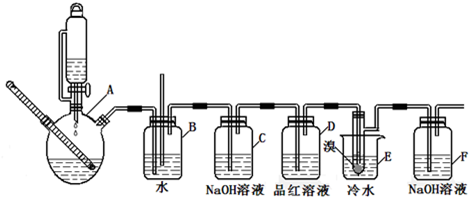
有关数据列表如表:
(1)A中药品为1:3的无水乙醇和浓硫酸混合液,写出制备乙烯的化学反应方程式: .
(2)气体发生装置使用连通滴液漏斗的原因 .
(3)装置D中品红溶液的作用是 ;同时B装置是安全瓶,监测实验进行时E中是否发生堵塞,请写出堵塞时的现象 .
(4)反应过程中应用冷水冷却装置E,其主要目的是 ;但又不能过度冷却(如用冰水),其原因是 .
(5)判断该制备反应已经结束的方法是 ;结果学生发现反应结束时,无水乙醇消耗量大大超过理论值,其原因是 .
(6)有学生提出,装置F中可改用足量的四氯化碳液体吸收多余的气体,判断改用四氯化碳液体是否可行 (填“是”或“否”),其原因是 .
0 60664 60672 60678 60682 60688 60690 60694 60700 60702 60708 60714 60718 60720 60724 60730 60732 60738 60742 60744 60748 60750 60754 60756 60758 60759 60760 60762 60763 60764 60766 60768 60772 60774 60778 60780 60784 60790 60792 60798 60802 60804 60808 60814 60820 60822 60828 60832 60834 60840 60844 60850 60858 203614

有关数据列表如表:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(2)气体发生装置使用连通滴液漏斗的原因
(3)装置D中品红溶液的作用是
(4)反应过程中应用冷水冷却装置E,其主要目的是
(5)判断该制备反应已经结束的方法是
(6)有学生提出,装置F中可改用足量的四氯化碳液体吸收多余的气体,判断改用四氯化碳液体是否可行
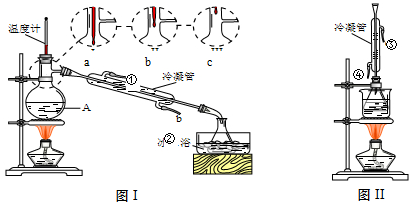
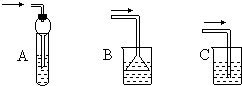 实验室在蒸馏烧瓶中加NaBr、适量水、95%的乙醇和浓硫酸,边反应边蒸馏,蒸出的溴乙烷用水下收集法获得.反应的化学方程式为:
实验室在蒸馏烧瓶中加NaBr、适量水、95%的乙醇和浓硫酸,边反应边蒸馏,蒸出的溴乙烷用水下收集法获得.反应的化学方程式为: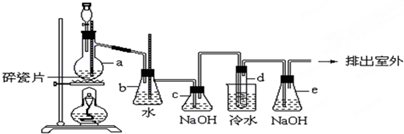
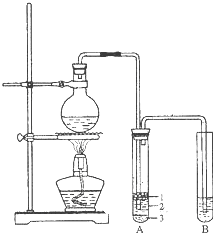 实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空:
实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空: