下列说法正确的是( )
| A、常温下物质的量浓度相等的①(NH4)2CO3 ②(NH4)2SO4 ③(NH4)2Fe(SO4)2三种溶液中水的电离程度:③>②>① | B、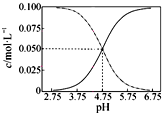 常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示,当pH=4.5溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) | C、向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2HCO3-+2OH-→CO32-+CaCO3↓+2H2O | D、25℃时,HCN溶液的电离平衡常数(Ka)与NaCN溶液的水解平衡常数(K)存在如下关系:Kw?K=Ka |
下列说法中,正确的是( )
| A、已知25℃时NH4CN水溶液显碱性,则25℃时的电离常数K(NH3?H2O)>K(HCN) | B、25℃时,Mg(OH)2固体在20 mL 0.01mol?L-1氨水中的Ksp比在20mL 0.01mol?L-1 NH4Cl溶液中的Ksp小 | C、pH试纸测得新制氯水的pH为4.5 | D、FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3 |
下列说法正确的是( )
| A、向50mL 1mol?L-1的盐酸中加入烧碱,水的KW不变 | ||
| B、NH4Cl和NH3?H2O混合液中,二者对对方的平衡都起了抑制作用 | ||
| C、有两种弱酸HX和HY且酸性HX>HY,则体积和浓度相同的NaX和NaY溶液中有c(Y-)>c(X-)>c(OH-)>c(H+) | ||
D、常温下0.1 mol?L-1的HA溶液中
|
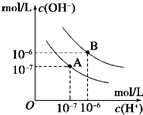 已知水在25℃和95℃时,其电离平衡曲线如图所示,下列说法错误的( )
已知水在25℃和95℃时,其电离平衡曲线如图所示,下列说法错误的( )| A、A曲线代表25℃时水的电离平衡曲线 | B、当95℃时,pH=6的溶液呈中性 | C、25℃时,将10mLpH=12的NaOH溶液与1mLpH=1的H2SO4溶液混合,所得溶液的pH=7 | D、95℃时,等体积等物质的量浓度的HA溶液和NaOH溶液混合后,当混合溶液的pH=6时,说明HA酸为弱酸 |
水是一种重要的资源,节约用水是“全民节约,共同行动”重要的一项.关于水的下列说法正确的是( )
| A、水可以电离出离子,所以是强电解质 | B、水的离子积可表示KW=c(H+)?c(OH-) | C、常温下水中的c(H+)大于c(OH-) | D、升高温度,c(H+)增大,显弱酸性 |
下列各项所给的两个量,前者一定小于后者的是( )
①纯水在25℃和80℃的pH;
②1moI NaHSO4和1mo1 Na2SO4在熔化状态下的离子数;
③25℃时,等体积且pH都等于3的盐酸和AlCl3的溶液中,已电离的水分子数;
④常温下,pH为10的氨水溶液和pH为12氨水溶液中所含溶质分子数.
①纯水在25℃和80℃的pH;
②1moI NaHSO4和1mo1 Na2SO4在熔化状态下的离子数;
③25℃时,等体积且pH都等于3的盐酸和AlCl3的溶液中,已电离的水分子数;
④常温下,pH为10的氨水溶液和pH为12氨水溶液中所含溶质分子数.
| A、①② | B、②④ | C、①③ | D、②③ |
室温下,水的电离达到平街:H2O?H++OH-.下列叙述正确的是( )
| A、将水加热,平衡向正向移动,KW变小 | B、向水中加入少量NaOH固体,平衡向逆向移动,c(OH-)增大 | C、新制氯水久置后,水的电离平衡向正向移动,c(OH-)增大 | D、向水中加入少量CH3COONa固体,平衡向正向移动,Kw增大 |
下列说法正确的是( )
| A、在蒸馏水中滴加浓H2SO4,Kw不变 | B、CaCO3难溶于稀硫酸,也难溶于醋酸 | C、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | D、在Na2S稀溶液中,c(H+)-c(OH-)=c(HS-)+2c(S2-)-c(Na+) |
下列说法正确的是( )
| A、水的离子积常数KW随温度改变而改变,随外加酸碱浓度改变而改变 | B、一元弱酸的电离常数Ka越小,表示此温度下该一元弱酸电离程度越大 | C、对已达到化学平衡的反应,仅改变浓度,若平衡移动则平衡常数(K)一定改变 | D、Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
室温下,下列各选项中所述的两个量,前者一定大于后者的是( )
| A、pH=10的NaOH和Na2CO3溶液中,水的电离程度 | B、将pH=3的盐酸和醋酸分别稀释成pH=5的溶液,需加水的体积 | C、10mL0.1 mol?L-1的醋酸与100mL 0.01 mol?L-1的醋酸中的H+物质的量 | D、物质的量浓度相等的(NH4)2SO4溶液与(NH4)2CO3溶液中NH4+的物质的量浓度 |