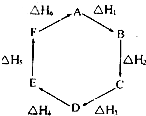
 盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与具体反应进行的途径无关.物质A在一定条件下可发生一系列转化,如图判断下列关系正确的是( )
盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与具体反应进行的途径无关.物质A在一定条件下可发生一系列转化,如图判断下列关系正确的是( )| A、A→F,△H=-△H 6 | B、△H1+△H 2+△H 3+△H 4+△H 5+△H 6=1 | C、C→F,△H=△H 1+△H 2+△H 6 | D、△H 1+△H 2+△H 3═△H 4+△H5+△H 6 |
一些物质的燃烧热如表:
则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
| 名称 | 化学式 | △H/(kJ?mol-1) |
| 一氧化碳 | CO(g) | -283.0 |
| 乙烯 | C2H4(g) | -1411.0 |
| 乙醇 | C2H5OH(l) | -1366.8 |
| A、-44.2 kJ?mol-1 |
| B、+44.2 kJ?mol-1 |
| C、-330 kJ?mol-1 |
| D、+330 kJ?mol-1 |
下列说法正确的是( )
| A、利用红外光谱可测定原子或基团的相对原子(分子)质量 | B、利用盖斯定律,可计算某些难以直接测量的反应的焓变 | C、沸点:AsH3>PH3>NH3,熔点:Si3N4>NaCl>SiCl4,酸性:HClO4>H2SO4>H3PO4 | D、蛋白质、油脂、PE、淀粉、醋酸纤维均为可水解的高分子化合物 |
强酸和强碱在稀溶液中的中和热可表示为:H+(aq)+OH-(aq)=H2O(l);△H=-57.3k kJ?mol-1,又知在溶液中反应有:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l);△H1=-Q1kJ?mol-1,
H2SO4(浓)+NaOH(aq)=
Na2SO4(aq)+H2O(l);△H2=-Q2 kJ?mol-1
HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(l);△H3=-Q3 kJ?mol-1,
则△H1、△H2、△H3的关系正确的是( )
| 1 |
| 2 |
| 1 |
| 2 |
HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(l);△H3=-Q3 kJ?mol-1,
则△H1、△H2、△H3的关系正确的是( )
| A、△H1=△H2=△H3 |
| B、△H2>△H1>△H3 |
| C、△H1>△H3>△H2 |
| D、△H2=△H3>△H1 |
已知:①CO(g)+
O2(g)═CO2(g)△H=-283.0kJ?mol-1②H2(g)+
O2(g)═H2O(g)△H=-241.8kJ?mol-1,则CO(g)+H2O(g)═H2(g)+CO2(g)的△H为( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、+41.2 kJ?mol-1 |
| B、-41.2 kJ?mol-1 |
| C、+82.4kJ?mol-1 |
| D、-524.8 kJ?mol-1 |
已知在25℃时:2C(s)+O2(g)=2CO(g)△H1=-222kJ/mol
2H2(g)+O2(g)=2H2O(g)△H2=-484kJ/mol
C(s)+O2(g)=CO2(g)△H3=-394kJ/mol
则25℃时,CO(g)+H2O(g)=CO2(g)+H2(g)的反应热△H4为( )
2H2(g)+O2(g)=2H2O(g)△H2=-484kJ/mol
C(s)+O2(g)=CO2(g)△H3=-394kJ/mol
则25℃时,CO(g)+H2O(g)=CO2(g)+H2(g)的反应热△H4为( )
| A、-82kJ/mol | B、-41kJ/mol | C、-312kJ/mol | D、+82kJ/mol |
已知:H2O(g)=H2O(l)△H1=-Q1kJ/mol;C2H5OH(g)=C2H5OH(l)△H2=-Q2kJ/mol;C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H3=-Q3kJ/mol.则酒精的燃烧热为( )
| A、2(Q1+Q2+Q3)kJ/mol | B、(Q1+Q2+Q3 ) kJ/mol | C、(Q1-Q2+Q3 )kJ/mol | D、(3Q1-Q2+Q3 ) kJ/mol |
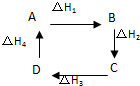 从起始状态下A出发,在一定条件下可发生一系列变化,由图判断下列关系错误的是( )
从起始状态下A出发,在一定条件下可发生一系列变化,由图判断下列关系错误的是( )| A、A→D,△H=-△H4 | B、△H1+△H2+△H3+△H4=0 | C、A→C,△H=△H3+△H4 | D、|△H2+△H3|=|△H1+△H4| |
已知:①2C(s)+O2(g)=2CO(g)△H=-221.0kJ/mol
②C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
则制备水煤气的反应C(s)+H2O(g)=CO(g)+H2(g)的△H为( )
②C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
则制备水煤气的反应C(s)+H2O(g)=CO(g)+H2(g)的△H为( )
| A、+131.3 kJ/mol | B、-131.3 kJ/mol | C、+373.1kJ/mol | D、-373.1 kJ/mol |
已知下列热化学方程式:
2Zn(s)+O2(g)=2ZnO(s)△H=-702.2kJ?mol-1
Hg(l)+
O2(g)=HgO(s)△H=-90.7kJ?mol-1
由此可知Zn(s)+HgO(s)=ZnO(s)+Hg(l)的反应热△H为( )
2Zn(s)+O2(g)=2ZnO(s)△H=-702.2kJ?mol-1
Hg(l)+
| 1 |
| 2 |
由此可知Zn(s)+HgO(s)=ZnO(s)+Hg(l)的反应热△H为( )
| A、-260.4kJ?mol-1 |
| B、+260.4kJ?mol-1 |
| C、-611.5kJ?mol-1 |
| D、+520.8kJ?mol-1 |