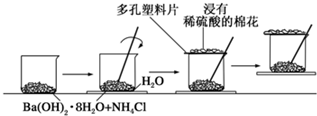
盖斯定律认为:不管化学过程是一步完成或分为数步完成,这个过程的热效应是相同的.
已知:H2O(g)=H2O(l)△H1=-Q1kJ?mol-1(Q1>0)
C2H5OH(g)=C2H5OH(l)△H2=-Q2kJ?mol-1(Q2>0)
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H3=-Q3kJ?mol-1(Q3>0)
若使23g液态乙醇完全燃烧,最后恢复到室温,则放出的热量为(kJ)( )
已知:H2O(g)=H2O(l)△H1=-Q1kJ?mol-1(Q1>0)
C2H5OH(g)=C2H5OH(l)△H2=-Q2kJ?mol-1(Q2>0)
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H3=-Q3kJ?mol-1(Q3>0)
若使23g液态乙醇完全燃烧,最后恢复到室温,则放出的热量为(kJ)( )
| A、Q1+Q2+Q3 | B、0.5(Q1+Q2+Q3) | C、0.5 Q1-1.5 Q2+0.5Q3 | D、1.5 Q1-0.5 Q2+0.5Q3 |
现有三个热化学方程式:则反应2C(s)+2H2(g)+O2(g)═CH3COOH(l) 的反应热为( )
(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
(3)H2(g)+
O2(g)═H2O(l)△H3=-285.8kJ/mol.
(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
(3)H2(g)+
| 1 |
| 2 |
| A、-488.3 kJ/mol |
| B、+488.3 kJ/mol |
| C、-2228.9 kJ/mol |
| D、+191 kJ/mol |
已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H1
2H2O2(l)═2H2O(l)+O2(g)△H2
2H2(g)+O2(g)═2H2O(l)△H3
则反应Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)的△H是( )
2H2O2(l)═2H2O(l)+O2(g)△H2
2H2(g)+O2(g)═2H2O(l)△H3
则反应Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)的△H是( )
A、△H=△H1+
| ||||
B、△H=△H1+
| ||||
| C、△H=△H1+2△H2+2△H3 | ||||
| D、△H=2△H1+△H2+△H3 |
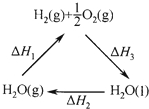 现在科学家正在寻求将太阳能转化成化学能,其中办法之一就是利用太阳能将H2O分解成H2,再将化学能转化为其它能源.如图是有关的能量循环示意图,下列有关说法正确的是( )
现在科学家正在寻求将太阳能转化成化学能,其中办法之一就是利用太阳能将H2O分解成H2,再将化学能转化为其它能源.如图是有关的能量循环示意图,下列有关说法正确的是( )| A、图中△H1=△H2+△H3 | B、如果H-H的键能为a kJ/mol,o=o键能为b kJ/mol,则断开1mol H-O键所需要的太阳能为(△H1+a+b)kJ | C、H2燃烧热为△H3 kJ/mol | D、水蒸气所具有的能量比液态水多△H2 kJ |
在1200℃时,天然气脱硫工艺中会发生下列反应:
H2S(g)+
O2(g)═SO2(g)+H2O(g)△H1
2H2S(g)+SO2(g)═
S2(g)+2H2O(g)△H2
H2S(g)+
O2(g)═S(g)+H2O(g)△H3
2S(g)═S2(g)△H4
则△H4的正确表达式为( )
H2S(g)+
| 3 |
| 2 |
2H2S(g)+SO2(g)═
| 3 |
| 2 |
H2S(g)+
| 1 |
| 2 |
2S(g)═S2(g)△H4
则△H4的正确表达式为( )
A、△H4=
| ||
B、△H4=
| ||
C、△H4=
| ||
D、△H4=
|