已知A和B为第三周期元素,其第一至第四电离能如下表所示:
(1)A通常显 价,B的基态原子核外电子排布式为 .
(2)H2O的熔沸点高于H2S,其主要原因是 .
(3)CH2=CH-C≡CH分子中的σ键与π键的键数之比为 .
| 电离能(I)/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)H2O的熔沸点高于H2S,其主要原因是
(3)CH2=CH-C≡CH分子中的σ键与π键的键数之比为
请根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是 .
| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能 (kJ/mol) |
1681 | 1251 | 1140 | 1008 | 900 |
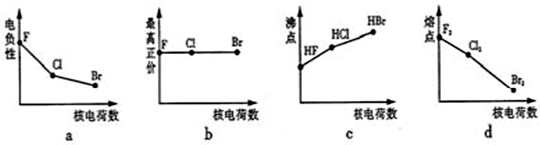
美国化学家鲍林(L.Pauling)首先提出了电负性的概念.电负性也是元素的一种重要性质,电负性越大,其原子吸引电子的能力越强,在所形成的分子中成为带负电荷的一方.下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,试回答下列问题:
(1)同主族的不同元素的电负性变化的规律是: 同周期中不同元素的电负性变化的规律是:
(2)预测周期表中,电负性最小的元素位于第 周期 族(放射性元素除外).
0 60503 60511 60517 60521 60527 60529 60533 60539 60541 60547 60553 60557 60559 60563 60569 60571 60577 60581 60583 60587 60589 60593 60595 60597 60598 60599 60601 60602 60603 60605 60607 60611 60613 60617 60619 60623 60629 60631 60637 60641 60643 60647 60653 60659 60661 60667 60671 60673 60679 60683 60689 60697 203614
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 | 0.8 |
(1)同主族的不同元素的电负性变化的规律是:
(2)预测周期表中,电负性最小的元素位于第
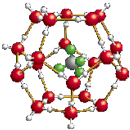 我国在青藏高原发现大储量可燃冰.可燃冰的晶体结构模型如图:
我国在青藏高原发现大储量可燃冰.可燃冰的晶体结构模型如图: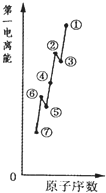 物质结构的多样性让人类使用的材料精彩纷呈.
物质结构的多样性让人类使用的材料精彩纷呈.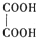 ,草酸钠晶体中存在
,草酸钠晶体中存在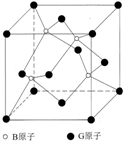 现有aA、bB、cC、dD、eE、gG六种短周期元素,a+b=c,a+c=d,a+d=e,d+e=g,B、C、E、G的单质均有多种同素异形体,请回答下列问题:
现有aA、bB、cC、dD、eE、gG六种短周期元素,a+b=c,a+c=d,a+d=e,d+e=g,B、C、E、G的单质均有多种同素异形体,请回答下列问题: