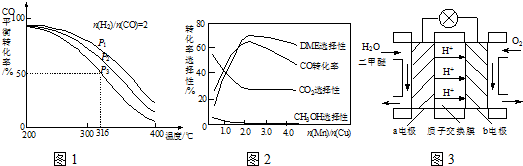
二甲醚是一种重要的清洁燃料,工业上可利用煤的气化产物(水煤气)合成二甲醚.利用水煤气合成二甲醚的热化学方程式为:
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-274kJ?mol-1.
(1)该反应在一定条件下的密闭容器中达到平衡后,为同时提高反应速率和二甲醚的产率,可以采取的措施是 (填字母)
A.降低温度 B.加入催化剂 C.缩小容器体积 D.增加H2的浓度 E.分离出二甲醚
(2)该反应可以分两步进行:
4H2(g)+2CO(g)═CH3OCH3(g)+H2O(g)△H1 ①
CO(g)+H2O(g)═CO2(g)+H2△H2=-42kJ?mol-1
则反应①的焓变△H1= kJ?mol-1,熵变△S (填“>、<或=”)0.
已知某些化学键的键能数据如下表所示:
CO中C与O之间为叁键连接,则CO2中碳氧键的键能是 kJ?mol-1.
(3)二甲醚也可以通过CH3OH分子间脱水制得:
2CH3OH(g)?CH3OCH3(g)+H2O(g)△H3=-23.5kJ?mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度变化如下表:
①该条件下反应平衡常数K= .
②相同条件下,若改变起始浓度.
此时正、逆反应速率的大小:v正 (填“>、<或=”)v逆.
(4)二甲醚-空气是一种高效的燃料电池,在氢氧化钾溶液中,电池反应方程式为:
CH3OCH3(l)+3O2(g)+4KOH(aq)═2K2CO3(aq)+5H2O(l)
请写出负极的电极反应式: .
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-274kJ?mol-1.
(1)该反应在一定条件下的密闭容器中达到平衡后,为同时提高反应速率和二甲醚的产率,可以采取的措施是
A.降低温度 B.加入催化剂 C.缩小容器体积 D.增加H2的浓度 E.分离出二甲醚
(2)该反应可以分两步进行:
4H2(g)+2CO(g)═CH3OCH3(g)+H2O(g)△H1 ①
CO(g)+H2O(g)═CO2(g)+H2△H2=-42kJ?mol-1
则反应①的焓变△H1=
已知某些化学键的键能数据如下表所示:
| 化学键 | C-H | O-H | H-H | C-O | C≡O |
| 键能/kJ.mol-1 | 413 | 463 | 436 | 358 | 1072 |
(3)二甲醚也可以通过CH3OH分子间脱水制得:
2CH3OH(g)?CH3OCH3(g)+H2O(g)△H3=-23.5kJ?mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度变化如下表:
| 物质 | CH3OH (g) | CH3OCH3 (g) | H2O (g) |
| 起始浓度/mol.l-1 | 2 | 0.2 | 0 |
| 平衡浓度/mol.l-1 | 0.4 | 1 | 0.8 |
②相同条件下,若改变起始浓度.
| 物质 | CH3OH (g) | CH3OCH3 (g) | H2O (g) |
| 起始浓度/mol.l-1 | 0.4 | 1.2 | 0.6 |
(4)二甲醚-空气是一种高效的燃料电池,在氢氧化钾溶液中,电池反应方程式为:
CH3OCH3(l)+3O2(g)+4KOH(aq)═2K2CO3(aq)+5H2O(l)
请写出负极的电极反应式:
近年来,各国加速推进燃料电池的研发.燃料电池的燃料有氢气、甲醇等.
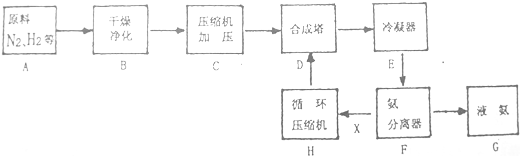
(1)通过下列硫--碘循环工艺可制得燃料电池的燃料氢气:
①该循环工艺过程的总反应方程式为 .
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是
(2)二氧化碳是地球温室效应的罪魁祸首,目前人们处理二氧化碳的方法之一是使其与氢气反应合成甲醇.已知氢气、甲醇燃烧的热化学方程式如下:
2H2(g)+O2(g)=2H2O(l);△H=-283.0kJ?mol-1…①
2CH3OH(1)+3O2(g)→2CO2(g)+4H2O(1);△H=-726.0kJ?mol-1…②
写出二氧化碳与氢气合成甲醇液体的热化学方程式 .
(3)甲醇--空气燃料电池是利用稀土金属氧化物作为固体电解质,这种稀土金属氧化物在高温下能传导O2-.
①负极发生的反应是
②在稀土金属氧化物的固体电解质中,O2-.的移动方向是 .
(4)已知反应2CH30H?CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此 温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小v正 v逆 (填“>”、“<”或“=”).
②若加入CH3OH后,经10min反应达到平衡,该时间内反应速率v(CH30H)= .
(1)通过下列硫--碘循环工艺可制得燃料电池的燃料氢气:

①该循环工艺过程的总反应方程式为
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是
(2)二氧化碳是地球温室效应的罪魁祸首,目前人们处理二氧化碳的方法之一是使其与氢气反应合成甲醇.已知氢气、甲醇燃烧的热化学方程式如下:
2H2(g)+O2(g)=2H2O(l);△H=-283.0kJ?mol-1…①
2CH3OH(1)+3O2(g)→2CO2(g)+4H2O(1);△H=-726.0kJ?mol-1…②
写出二氧化碳与氢气合成甲醇液体的热化学方程式
(3)甲醇--空气燃料电池是利用稀土金属氧化物作为固体电解质,这种稀土金属氧化物在高温下能传导O2-.
①负极发生的反应是
②在稀土金属氧化物的固体电解质中,O2-.的移动方向是
(4)已知反应2CH30H?CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此 温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L-1) | 0.44 | 0.6 | 0.6 |
②若加入CH3OH后,经10min反应达到平衡,该时间内反应速率v(CH30H)=
工业生产硫酸中,用硫铁矿煅烧产生SO2,为了提高SO2的生成速率,下列措施可行的是( )
| A、把硫铁矿石由小块碾成粉末 | B、增大O2压强,向炉内喷吹氧气 | C、使用Fe2O3作催化剂 | D、降低温度 |
工业上用硫酸和废铁屑制备硫酸亚铁时,为了提高产品的质量,常采取的措施是( )
| A、硫酸过量 | B、铁屑过量 | C、硫酸和铁的物质的量之比为1:1 | D、需要用浓H2SO4 |
 目前,全国多个地区为雾霾所困,氮氧化物是造成雾霾天气的主要原因之一.消除氮氧化物有多种方法.在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染.
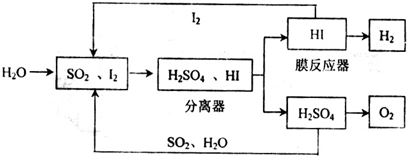
目前,全国多个地区为雾霾所困,氮氧化物是造成雾霾天气的主要原因之一.消除氮氧化物有多种方法.在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染.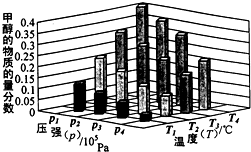 能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.