已知反2O3(g)=3O2(g)的△H<0、△S>0,对此反应叙述正确的是( )
| A、该反应在任何情况下均能自发进行 | B、该反应在任何情况下均不能自发进行 | C、该反应在高温能自发进行 | D、条件不足,无法判断 |
已知: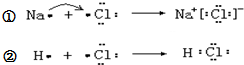 ,下列说法不正确的是( )
,下列说法不正确的是( )
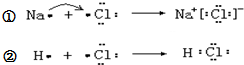 ,下列说法不正确的是( )
,下列说法不正确的是( )| A、①和②变化过程中都会放出热量 | B、氯原子吸引电子的能力强于钠原子和氢原子 | C、①和②中的氯原子均得到1个电子达到8电子稳定结构 | D、NaCl中含有离子键,HCl中含有共价键 |
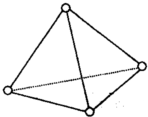 如图表示白磷(P4)分子结构.白磷在氧气不足时燃烧生成P4O6,P4O6分子结构可以看成是白磷分子中磷磷键之间插入氧原子.
如图表示白磷(P4)分子结构.白磷在氧气不足时燃烧生成P4O6,P4O6分子结构可以看成是白磷分子中磷磷键之间插入氧原子.已知:键能表示断裂1mol化学键需要吸收的能量.几种共价键的键能如表所示:
| 化学键 | P-P | P-O | P═O | O═O |
| 键能/kJ?mol-1 | a | b | c | d |
| A、(6a+3d-12b-4c)kJ?mol-1 |
| B、(4a+3d-8b)kJ?mol-1 |
| C、(6a+3d-12b)kJ?mol-1 |
| D、(6a+3d+4c-12b)kJ?mol-1 |
下列说法正确的是( )
| A、反应CaCO3(s)=CaO(s)+CO2(g)在常温下不能发生,则该反应的△H>0 | ||
B、0.1mol?L-1CH3COOH溶液加水稀释后,溶液中
| ||
| C、铅蓄电池在放电过程中,负极质量增加,正极质量减少 | ||
| D、锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去 |
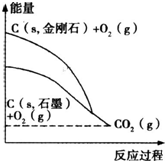 根据右图所示的各物质能量变化关系,判断下列热化学方程式正确的是( )
根据右图所示的各物质能量变化关系,判断下列热化学方程式正确的是( )| A、C(金刚石,s)+O2(g)=CO2(g)△H1=a kJ?mol-1 (a<0) | B、C(石墨,s)+O2(g)=CO2(g);△H2=b kJ?mol-1 (b>0) | C、C+O2=CO2(g)△H3=c kJ?mol-1 (c<0) | D、C(s,金刚石)=C(s,石墨)△H4=d kJ?mol-1 (d>0) |
下列叙述正确的是( )
| A、放热反应的生成物总能量高于反应物总能量 | B、乙醇可以被氧化为乙酸,二者都能发生酯化反应 | C、由多种非金属元素组成的化合物一定是共价化合物 | D、含5个碳原子的有机物,每个分子中最多可形成4个C-C单键 |
关于下列各图的叙述,正确的是( )
A、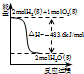 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ?mol-1 | B、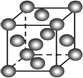 表示Cu形成金属晶体时的堆积方式 | C、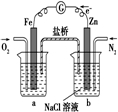 烧杯a中的溶液pH降低 | D、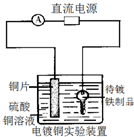 待镀铁制品应与电源正极相连 |
已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡,其相关热化学方程式为如图所示,下列说法正确的是( )
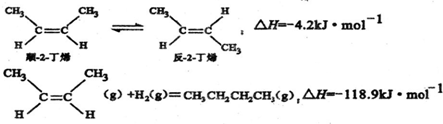

| A、顺-2-丁烯比反-2-丁烯稳定 | B、顺-2-丁烯的燃烧热数值比反-2-丁烯大 | C、顺-2-丁烯和反-2-丁烯分别与氢气加成后所得产物不同 | D、反-2-丁烯氢化的热化学方程式为: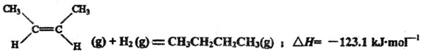 |
氯原子对O3的分解有催化作用:O3+Cl═ClO+O2△H1,ClO+O═Cl+O2△H2该反应的能量变化如图示意,下列叙述中正确的是( )
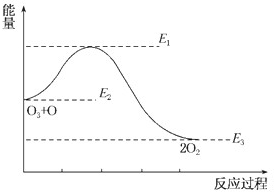

| A、反应O3+O═2O2的△H=E1-E2 | B、反应O3+O═2O2的△H=E2-E3 | C、反应O3+O═2O2是吸热反应 | D、反应O3+O═2O2的△H=△H1+△H2 |
下列图示与对应的叙述相符的是( )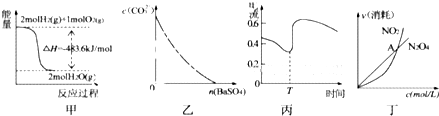

| A、图甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ?mol-1 | B、图乙表示在饱和Na2CO3溶液中逐步加BaSO4固体后,溶液中c(CO32-)的浓度变化 | C、图丙表示Zn、Cu和稀硫酸构成的原电池在工作过程中电流强度的变化,T时加入了H2O2 | D、图丁表示恒温恒容条件下发生的可逆反应2NO2?N202(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 |