题目内容
下列图示与对应的叙述相符的是( )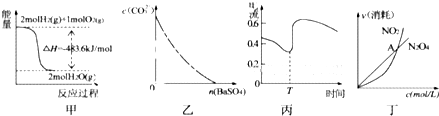

| A、图甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ?mol-1 | B、图乙表示在饱和Na2CO3溶液中逐步加BaSO4固体后,溶液中c(CO32-)的浓度变化 | C、图丙表示Zn、Cu和稀硫酸构成的原电池在工作过程中电流强度的变化,T时加入了H2O2 | D、图丁表示恒温恒容条件下发生的可逆反应2NO2?N202(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 |
分析:A、依据氢气的燃烧热概念和图象分析,燃烧热是1mol可燃物完全燃烧生成稳定氧化物过程中放出的热量为燃烧热分析判断;
B、饱和Na2CO3溶液中逐步加BaSO4固体后实现沉淀转化,碳酸钙离子浓度减小,但是建立的沉淀溶解和沉淀转化平衡状态,碳酸根离子不能减小为0;
C、Zn、Cu和稀硫酸构成的原电池在工作过程中,锌失电子发生氧化反应,随稀硫酸浓度减小反应进行,电流强度减小,T时加入了H2O2,是强氧化剂,可以加快锌溶解的反应,电流强度增大,随反应进行电流强度又减小,但比开始电流强度大;
D、可逆反应2NO2?N204(g)中,分析判断 二氧化氮消耗速率和四氧化二氮的消耗速率之比为2:1,说明反应达到平衡状态.
B、饱和Na2CO3溶液中逐步加BaSO4固体后实现沉淀转化,碳酸钙离子浓度减小,但是建立的沉淀溶解和沉淀转化平衡状态,碳酸根离子不能减小为0;
C、Zn、Cu和稀硫酸构成的原电池在工作过程中,锌失电子发生氧化反应,随稀硫酸浓度减小反应进行,电流强度减小,T时加入了H2O2,是强氧化剂,可以加快锌溶解的反应,电流强度增大,随反应进行电流强度又减小,但比开始电流强度大;
D、可逆反应2NO2?N204(g)中,分析判断 二氧化氮消耗速率和四氧化二氮的消耗速率之比为2:1,说明反应达到平衡状态.
解答:解:A、依据氢气的燃烧热概念和图象分析,燃烧热是1mol可燃物完全燃烧生成稳定氧化物过程中放出的热量为燃烧热,图象中生成的水是气体,反应热是2mol氢气燃烧放出的热量,故A错误;
B、饱和Na2CO3溶液中逐步加BaSO4固体后实现沉淀转化,碳酸钙离子浓度减小,但是建立的沉淀溶解和沉淀转化平衡状态,碳酸根离子不能减小为0,故B错误;
C、Zn、Cu和稀硫酸构成的原电池在工作过程中,锌失电子发生氧化反应,随稀硫酸浓度减小反应进行,电流强度减小,T时加入了H2O2,是强氧化剂,可以加快锌溶解的反应,电流强度增大,随反应进行电流强度又减小,但比开始电流强度大,故C正确;
D、可逆反应2NO2?N204(g)中,分析判断,二氧化氮消耗速率和四氧化二氮的消耗速率之比为2:1时才能说明反应达到平衡状态,交点只是浓度相同不能证明达到终点,故D错误;
故选C.
B、饱和Na2CO3溶液中逐步加BaSO4固体后实现沉淀转化,碳酸钙离子浓度减小,但是建立的沉淀溶解和沉淀转化平衡状态,碳酸根离子不能减小为0,故B错误;
C、Zn、Cu和稀硫酸构成的原电池在工作过程中,锌失电子发生氧化反应,随稀硫酸浓度减小反应进行,电流强度减小,T时加入了H2O2,是强氧化剂,可以加快锌溶解的反应,电流强度增大,随反应进行电流强度又减小,但比开始电流强度大,故C正确;
D、可逆反应2NO2?N204(g)中,分析判断,二氧化氮消耗速率和四氧化二氮的消耗速率之比为2:1时才能说明反应达到平衡状态,交点只是浓度相同不能证明达到终点,故D错误;
故选C.
点评:本题考查了燃烧热概念和图象分析判断,沉淀转化关系分析,原电池原来的应用理解,化学平衡标志判断的应用,题目难度中等.

练习册系列答案
相关题目
下列图示与对应的叙述一定正确的是( )
A、图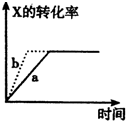 所示,反应:X(g)+2Y(g)?3Z(g),b的压强一定比a大 所示,反应:X(g)+2Y(g)?3Z(g),b的压强一定比a大 | B、图 表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 | C、图 所示,t1℃时质量分数均为20%的甲乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 所示,t1℃时质量分数均为20%的甲乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 | D、图 所示,用水稀释PH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a 所示,用水稀释PH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a |


