短周期元素R、T、Q、W、G在元素周期表中的相对位置如下图所示,其中Q是无机非金属材料的主角.下列判断正确的是( )
| R | ||||
| T | Q | W | G | |
| A、离子半径:T<W<G |
| B、最简单气态氢化物的热稳定性:Q<R |
| C、最高价氧化物对应水化物的酸性:Q>W>G |
| D、T和G组成的化合物甲溶于水,其水溶液呈中性 |
短周期元素X,Y,Z,W在周期表中相对位置如图所示,Y元素在地壳中的含量最高.下列说法正确的是( )
| X | Y | ||
| Z | W |
| A、原子半径;Z<Y<W |
| B、最简单气态氢化物的热稳定性:Y<W |
| C、含X的化合物形成的溶液一定呈酸性 |
| D、X的最简单阴离子和Z的最简单阳离子核外电子数相同 |
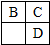 A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示.A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )
A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示.A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )| A、简单离子的半径大小关系:B>C>E | B、C元素的气态氢化物比D元素的气态氢化物稳定是氢键的缘故 | C、由A、B两种元素组成的离子化合物NH5中,阴、阳离子个数比为1:1 | D、由C、D、E三种元素组成的某种化合物,其水溶液能与盐酸反应产生沉淀 |
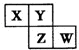 X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍.下列说法正确的是( )
X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍.下列说法正确的是( )| A、X、Y、Z的原子半径大小:X>Y>Z | B、Y的单质与氢气反应较Z剧烈 | C、Z、W的最高价氧化物对应水化物的酸性,前者更强 | D、X、W的气态氢化物能相互反应,生成共价化合物 |
下列说法中正确的是( )
①CO2与CS2互为等电子体;
②同一周期从左到右,元素的电负性、原子的半径都是越来越大;
③价电子数等于族序数;
④含有阳离子的晶体一定是离子晶体;
⑤温度越高,金属的导电性越好;
⑥熔融状态下能导电的化合物一定是离子晶体;
⑦P4和CH4都是正四面体分子且键角都为109°28ˊ.
①CO2与CS2互为等电子体;
②同一周期从左到右,元素的电负性、原子的半径都是越来越大;
③价电子数等于族序数;
④含有阳离子的晶体一定是离子晶体;
⑤温度越高,金属的导电性越好;
⑥熔融状态下能导电的化合物一定是离子晶体;
⑦P4和CH4都是正四面体分子且键角都为109°28ˊ.
| A、①②③ | B、⑤⑥⑦ | C、①④⑥⑦ | D、①⑥ |
应用元素周期律分析下列推断,其中正确的组合是( )
①碱金属单质的熔点随原子序数的增大而降低
②Cs是第ⅠA族元素,Cs失电子能力比Na的强
③砹(At)是第VIIA族,其氢化物的稳定性大于HCl
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱.
①碱金属单质的熔点随原子序数的增大而降低
②Cs是第ⅠA族元素,Cs失电子能力比Na的强
③砹(At)是第VIIA族,其氢化物的稳定性大于HCl
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱.
| A、①③⑤ | B、①②⑤ | C、②③⑤ | D、①②④ |
下列叙述正确的是( )
| A、同周期元素的离子半径从左到右逐渐减小 | B、同主族元素的离子半径从上到下逐渐增大 | C、同周期元素从左到右,金属性逐渐增强,非金属性逐渐减弱 | D、同主族元素的单质的熔点从上到下逐渐升高 |
下列排序正确的是( )
| A、热稳定性:H2O>HF>H2S | B、碱性:Mg(OH)2>Al(OH)3 | C、酸性:H2CO3>H3PO4>H2SO4 | D、原子半径:N>C |
不能用于判断金属失电子能力强弱的是( )
| A、同主族金属元素原子半径大小 | B、1mol金属单质在反应中失去电子的多少 | C、水溶液中金属间发生的置换反应 | D、金属元素最高价氧化物对应水化物的碱性强弱 |
在通常条件下,下列各组物质的性质排列顺序正确的是( )
| A、热稳定性:HF>H2O>NH3 | B、水溶性:HCl>NH3>SO2 | C、金属的原子化热:Al<Mg<Na | D、熔点:CO2>KCl>SiO2 |