将足量铁粉投入一定浓度的氯化铁和氯化铜的混合溶液中,充分反应后,溶液中剩余固体的质量与加入铁粉的质量相同,则原溶液中氯化铁和氯化铜的浓度之比为( )
| A、2:7 | B、3:4 | C、4:7 | D、2:3 |
下列有关含铜化合物的说法错误的是(设NA为阿伏加德罗常数的值)( )
| A、用盐酸可以洗去铜表面的铜锈 | B、0.1mol?L-1的CuSO4溶液中,Cu2+的数目一定小于0.1NA | C、在CuCl2和FeCl3的混合溶液中加入铁粉,若有固体残留,则其中一定含有铜 | D、在FeSO4溶液中加入CuS固体,溶液中c(Fe2+)不变,说明K甲(CuS)远小于K甲(FeS) |
(1)向FeCl3溶液中加入a g的铜粉,搅拌使之全部溶解,溶液中一定有的阳离子是 .可能有的阳离子是 .发生反应的离子方程式为 ;再向其中加入 b g铁粉,充分反应后过滤得滤渣c g,可能发生反应的离子方程式为 .若已知 a>b>c,则 c克滤渣是 .
(2)鉴别Na2SO3溶液和稀H2SO4.请按要求完成下表:
说明:第3步不能使用其他任何仪器(包括胶头滴管)和试剂.
(2)鉴别Na2SO3溶液和稀H2SO4.请按要求完成下表:
| 步骤 | 操作 | 现象及结论 |
| 1 | 用甲、乙两支试管分别取两种溶液各少许. | |
| 2 | 用胶头滴管向甲、乙试管中逐滴滴加BaCl2溶液至过量. | |
| 3 |
已知溴水和氯化铁溶液浓度较小时,溶液均显黄色.某同学将溴水和FeCl2溶液混合后,发现溶液显黄色.为探究溴水和FeCl2溶液是否反应,设计了以下实验方案:
请回答下列问题:
(1)方案1的结论是否合理? (填“合理”或“不合理”);
(2)方案2的结论明显不合理,写出其中可能发生反应的离子方程式 ;
(3)请你设计一个简单的实验方案,判断溴水和FeCl2溶液是否反应(写出实验操作、实验现象和结论):
.
0 59840 59848 59854 59858 59864 59866 59870 59876 59878 59884 59890 59894 59896 59900 59906 59908 59914 59918 59920 59924 59926 59930 59932 59934 59935 59936 59938 59939 59940 59942 59944 59948 59950 59954 59956 59960 59966 59968 59974 59978 59980 59984 59990 59996 59998 60004 60008 60010 60016 60020 60026 60034 203614
| 实验操作 | 实验现象 | 结论 | |
| 方案1 | 取少量混合溶液,加入NaOH溶液 | 最终得到红褐色沉淀, | 溴水和FeCl2溶液发生了化学反应 |
| 方案2 | 取少量混合溶液,加入淀粉碘化钾溶液 | 溶液变蓝色 | 溴水和FeCl2溶液未发生化学反应 |
(1)方案1的结论是否合理?
(2)方案2的结论明显不合理,写出其中可能发生反应的离子方程式
(3)请你设计一个简单的实验方案,判断溴水和FeCl2溶液是否反应(写出实验操作、实验现象和结论):
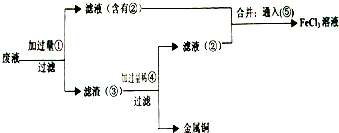
 铁及其化合物之间的相互转化可用下式表示:①②③④
铁及其化合物之间的相互转化可用下式表示:①②③④