下列金属化合物中最方便用于潜水艇舱内供氧的是( )
| A、KMnO4 | B、KClO3 | C、KNO3 | D、Na2O2 |
将含等物质的量的氯化铵和碳酸氢钠混合溶液蒸干灼烧最终得到的固体是( )
| A、只有碳酸钠 | B、只有氯化钠 | C、一定是氯化钠和碳酸钠的混合物 | D、碳酸铵 |
NA代表阿伏加德罗常数.常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28g,对该反应的分析,错误的是( )
| A、反应前后物质中阴、阳离子数目保持不变 | B、反应前后总物质的量减少0.5mol | C、反应中转移了NA电子并生成了11.2L氧气 | D、反应的二氧化碳和生成的氧气体积比为2:1 |
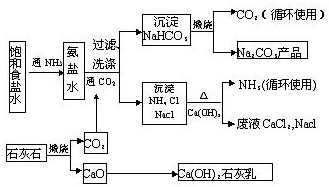
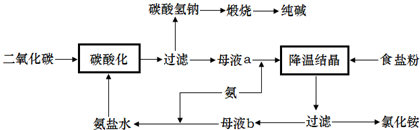
某研究性学习小组根据侯德榜制碱法原理并参考下表有关物质溶解度(g/100g水)数据,以饱和NaCl溶液与研细的NH4HCO3为原料,设计实验经两步反应制备纯碱.
下列有关说法中,正确的是( )
| 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | 35℃以上分解 | |||
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
| A、第一、二步反应的基本类型为化合反应、分解反应 |
| B、第一、二步反应之间的主要实验操作是过滤、洗涤 |
| C、第一步反应控制温度高于30℃目的是提高反应产率 |
| D、反应液加盐酸处理可使NaCl循环使用并回收NH4Cl |
下列关于工业生产的叙述中,错误的是( )
| A、用离子交换膜法电解饱和食盐水制烧碱 | B、目前合成氨,没有采用更高温度、更大压强是从设备和动力要求方面考虑的 | C、采用电解熔融氯化铝的方法制取金属铝 | D、生产硫酸时,接触室内热交换器的作用是预热进入的炉气和冷却反应生成的气体 |
在复习元素周期律过程中,某研究性学习小组的几位同学拟通过具体的实验来探讨某些金属元素的性质差异,下面是他们设计的探究性实验方案,请填写下列空白:
实验目的:比较钠、镁、铝金属性强弱.
实验用品:酒精灯、 、试管、试管夹、砂纸、滤纸;钠、镁条、铝片、酚酞、蒸馏水、6mol?L-1的盐酸
实验过程与现象记录:
I.甲同学的方案如表:
①你认为a、b两步实验中出现异常现象的可能原因是:a ;b .
②上面的实验表明:钠、镁、铝三种元素的金属性由强到弱的顺序为 .
II乙同学的方案:他认为只需要一种试剂就可以确定钠、镁、铝的金属性强弱,预计他的主要实验操作是 .
实验目的:比较钠、镁、铝金属性强弱.
实验用品:酒精灯、
实验过程与现象记录:
I.甲同学的方案如表:
| 实验过程 | 预期现象 | 实际观察到的现象 |
| a取已切去表皮的一小块金属钠,放入盛有水的某容器中 | 立即剧烈反应 |
开始时钠块浮在水面上不反应,稍后才开始与水剧烈反应 |
| b向盛有适量水(内含2滴 酚酞的试管中加入一小段镁条 |
有气泡产生,溶液变红色 | 没有相应现象,加热后仍无明显变化 |
| c向两支盛有3mL6mol?L-1盐酸的试管中加入大小相同的镁片和铝片 | 镁、铝与盐酸反应产生气泡剧烈程度不同 | 镁与盐酸反应产生气泡速率较快 |
②上面的实验表明:钠、镁、铝三种元素的金属性由强到弱的顺序为
II乙同学的方案:他认为只需要一种试剂就可以确定钠、镁、铝的金属性强弱,预计他的主要实验操作是
向氧化铜和铁粉的混合物中,加入一定量的稀硫酸,反应停止后,过滤,除去不溶物.向滤液中加一铁片,未看到铁片有任何变化.下列分析正确的是( )
| A、滤出的不溶物中一定含有Cu和Fe | B、滤出的不溶物中一定含有Cu | C、滤液中一定不含有CuSO4和FeSO4 | D、滤液中一定不含有CuSO4和H2SO4 |