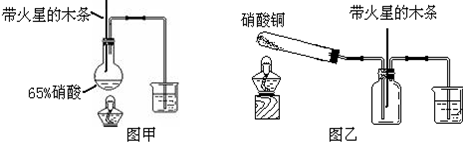
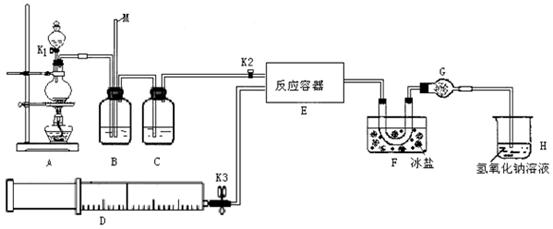
题目内容
| 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | 35℃以上分解 | |||
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
| A、第一、二步反应的基本类型为化合反应、分解反应 |
| B、第一、二步反应之间的主要实验操作是过滤、洗涤 |
| C、第一步反应控制温度高于30℃目的是提高反应产率 |
| D、反应液加盐酸处理可使NaCl循环使用并回收NH4Cl |
| ||
B、根据侯氏制碱法的制备步骤判断;
C、温度高于30℃,是为了提高碳酸氢铵的溶解度;
D、温度过高造成NH4HCO3分解.
| ||
B、第一、二步反应之间的主要实验操作是过滤、洗涤,故B正确;
C、温度过低NH4HCO3的溶解度小,温度高于30℃是为了提高碳酸氢铵的溶解度,故C错误;
D、反应液加盐酸处理,可以生成氯化钠晶体,得到了氯化铵溶液,故D正确;
故选BD.

(14分)亚硝酰氯(ClNO)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到。亚硝酰氯有关性质如下:
| 分子式 | 别名 | 熔点 | 沸点 | 溶解性 | 性状 |
| ClNO | 氯化亚硝酰 | -64.5℃ | -5.5℃ | 溶于浓硫酸 | 红褐色液体或有毒气体,具有刺激恶臭,遇水反应生成氮的氧化物与氯化氢 |
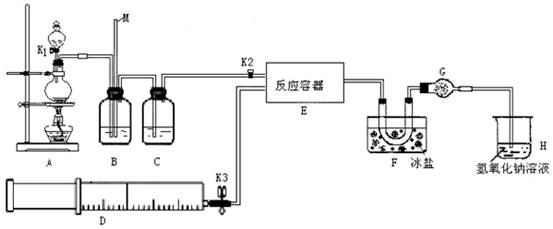
某研究性学习小组根据亚硝酰氯性质拟在通风橱中制取亚硝酰氯,设计了如图所示实验装置。实验开始前K2处于打开状态,K1、K3均已关闭。、
试回答下列问题:
(1)①若D中装有纯净的NO气体,则B中应选用的试剂为 。实验时利用B除去某些杂质气体并通过观察B中的气泡来判断反应速率,B还具有的作用是 ;②若D中装有纯净的氯气,则C中应选用的试剂为 。
(2)装置F的作用是 ;装置G的作用是 。
(3)若无装置G,则F中ClNO可能发生反应的化学方程式为 。
(4)某同学认为氢氧化钠溶液只能吸收氯气和ClNO,但不能吸收NO,所以装置H不能有效除去有毒气体。为解决这一问题,可将尾气与某种气体同时通入氢氧化钠溶液中,这种气体的化学式是 。
(14分)亚硝酰氯(ClNO)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到。亚硝酰氯有关性质如下:
|
分子式 |
别名 |
熔点 |
沸点 |
溶解性 |
性状 |
|
ClNO |
氯化亚硝酰 |
-64.5℃ |
-5.5℃ |
溶于浓硫酸 |
红褐色液体或有毒气体,具有刺激恶臭,遇水反应生成氮的氧化物与氯化氢 |
某研究性学习小组根据亚硝酰氯性质拟在通风橱中制取亚硝酰氯,设计了如图所示实验装置。实验开始前K2处于打开状态,K1、K3均已关闭。、
试回答下列问题:
(1)①若D中装有纯净的NO气体,则B中应选用的试剂为 。实验时利用B除去某些杂质气体并通过观察B中的气泡来判断反应速率,B还具有的作用是 ;②若D中装有纯净的氯气,则C中应选用的试剂为 。
(2)装置F的作用是 ;装置G的作用是 。
(3)若无装置G,则F中ClNO可能发生反应的化学方程式为 。
(4)某同学认为氢氧化钠溶液只能吸收氯气和ClNO,但不能吸收NO,所以装置H不能有效除去有毒气体。为解决这一问题,可将尾气与某种气体同时通入氢氧化钠溶液中,这种气体的化学式是 。