做实验时不小心粘在皮肤上的高锰酸钾会形成黑斑,很久才能消除,若用乙二酸的稀溶液擦洗黑斑,黑斑可以迅速褪去,其离子反应方程式为MnO
+H2C2O4+H+→CO2↑+Mn2++( )下列有关废反应的叙述正确的是( )
- 4 |
| A、乙二酸中C显+2价 |
| B、离子反应方程式右侧方框内的产物是OH- |
| C、氧化剂和还原剂的化学计量数之比是5:2 |
| D、若有6 mol H+参加反应,则转移电子10 mol |
在硫酸铁电化浸出黄铜矿精矿工艺中,有一主要反应:CuFeS2+4Fe3+═Cu2++5Fe2++2S,反应结束后,经处理获得单质硫x mol.下列说法正确的是( )
| A、反应中硫元素被氧化,所有铁元素均被还原 | B、氧化剂是Fe3+,氧化产物是Cu2+ | C、反应中转移电子的物质的量为xmol | D、反应结束后,测得溶液中三种金属离子的总物质的量为ymol,则原Fe3+的总物质的量为(y-x)mol |
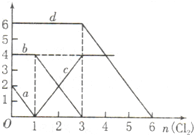 向FeBr2、FeI2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示,下列有关说法中不正确的是( )
向FeBr2、FeI2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示,下列有关说法中不正确的是( )| A、d曲线代表溶液中Br-变化情况 | B、原溶液中FeI2的物质的量为2mol | C、原溶液中n(Fe2+):n(Br-)=2:3 | D、当通入2mol Cl2时,溶液中离子反应为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
含有a mol FeBr2的溶液中,通入x mol Cl2.下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是( )
| A、x=0.3a,2Fe2++Cl2→2Fe3++2Cl- | B、x=0.7a,2Br-+Cl2→Br2+2Cl- | C、x=1.2a,2Fe2++2Br-+2Cl2→Br2+2Fe3++4Cl- | D、x=1.5a,2Fe2++4Br-+3Cl2→2Br2+2Fe3++6Cl- |
单质硫在KOH的热溶液中发生歧化反应:3S+6KOH
2K2S+K2SO3+3H2O;若硫过量,进一步生成K2Sx(x≤5)和K2S2O3.将0.08mol单质硫与含0.06mol KOH的热溶液充分反应恰好生成a mol K2Sx和b mol K2S2O3,再加入足量KClO、KOH的混合溶液,硫元素全部转化为K2SO4,转移电子n mol.则以下正确的是( )
| △ |
| A、a=2b | B、x=2 |
| C、n=0.48 | D、b=0.02 |
某金属和硝酸反应,已知参加反应的被还原的硝酸和参加反应的硝酸的物质的量之比为1:6,若已知还原产物唯一,则还原产物为( )
| A、N2 | B、N2O | C、NO | D、NO2 |
一定质量的镁、铝合金与硝酸溶液恰好完全反应,得硝酸盐溶液和NO2、N2O4、NO的混合气体,这些气体与标准状况下3.36L氧气混合后通入水中,所有气体恰好完全被水吸收生成硝酸.若向所得硝酸盐溶液中加入2mol/L NaOH溶液至沉淀最多时停止加入,将所产生沉淀滤出,向滤液加水稀释至500ml,此时所得溶液物质的量浓度为( )
| A、0.5mol/L | B、1mol/L | C、1.2mol/L | D、2mol/L |
水热法制备Fe3O4纳米颗粒的总反应:3Fe2++2S2O32-+O2+xOH-→Fe3O4+S4O62-+2H2O,有关说法正确的是( )
| A、每转移1.5mol电子,有1.125mol Fe2+被氧化 | B、x=2 | C、Fe2+、S2O32-都是还原剂 | D、每生成1mol Fe3O4,转移电子2mol |
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,产物有HF、NO和HNO3.下列关于该反应的说法中,正确的是( )
| A、水蒸气在反应中被NF3氧化 | B、反应中氧化产物与还原产物的物质的量之比为1:2 | C、反应中生成22.4L NO气体时,转移电子的物质的量为1mol | D、NF3在空气中泄漏时没有明显现象,用石灰水溶液喷淋的方法可减少污染 |