下表是实验室制备气体的有关内容:
(1)上述气体中,从制备过程看,必须选择合适的氧化剂才能实现的是 (填气体的化学式);从反应原理看,明显不同于其它两种气体的是 (填气体的化学式);从收集方法来看,只能用一种方法收集的是 (填气体的化学式).
(2)根据表中所列实验原理,从图甲装置中选择合适的气体发生装置,将其选项填入表中相应编号的空格中.
(3)若用上述制备NH3的装置制备O2,则选择的试剂为 (填化学式);若用上述制备O2的装置制备
NH3,则选择的试剂的名称为 .
(4)若用排空气法收集Cl2,请画出气体收集装置图.
(5)有图乙所示无机物的转化关系,已知B和Y是上述三种气体中的两种.
a.当w为MnO2时,反应①不加热就能反应,反应④加热才能顺利进行,写出反应①的化学方程式.
b.当w为KMnO2时,反应①加热才能进行,反应④不加热就能进行,写出反应④的离子方程式. .
(6)已知Fe2++Br2=2Fe3++2Br-,现向100mL的FeBr2溶液中通入标准状况下Cl23.36L,充分反应后,测得溶液中Cl-与Br-的物质的量浓度相等(设通入Cl2前后溶液体积不变),则原FeBr2溶液中溶质的物质的量浓度为 .
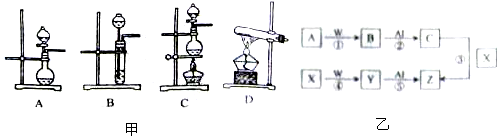
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制氧气 | H2O2→O2 | |
| ② | 制氨气 | NH4Cl→NH3 | |
| ③ | 制氯气 | HCl→Cl2 |
(2)根据表中所列实验原理,从图甲装置中选择合适的气体发生装置,将其选项填入表中相应编号的空格中.
(3)若用上述制备NH3的装置制备O2,则选择的试剂为
NH3,则选择的试剂的名称为
(4)若用排空气法收集Cl2,请画出气体收集装置图.
(5)有图乙所示无机物的转化关系,已知B和Y是上述三种气体中的两种.
a.当w为MnO2时,反应①不加热就能反应,反应④加热才能顺利进行,写出反应①的化学方程式.
b.当w为KMnO2时,反应①加热才能进行,反应④不加热就能进行,写出反应④的离子方程式.
(6)已知Fe2++Br2=2Fe3++2Br-,现向100mL的FeBr2溶液中通入标准状况下Cl23.36L,充分反应后,测得溶液中Cl-与Br-的物质的量浓度相等(设通入Cl2前后溶液体积不变),则原FeBr2溶液中溶质的物质的量浓度为

如图1所示是实验室中制取气体的一种简易装置.

(1)请简述检验它的气密性的方法.
(2)利用如图1所示装置制取气体时,可适用的反应条件和反应物状态为 .
某同学设计如图2所示装置,用粗铁粒与16.9%稀硝酸反应制取NO气体并探究产物中铁的价态.请回答有关问题.
(3)已知16.9%稀硝酸的密度为1.10g?cm-3,则其物质的量浓度为 (计算结果保留两位小数).若用63%的硝酸配制16.9%稀硝酸500mL,所需的玻璃仪器有量筒、玻璃棒、烧杯、 .
(4)实验开始时,先打开止水夹a、关闭止水夹b时,A装置的干燥管中观察到的现象是 .B装置烧杯中液体的作用是 .当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体.
(5)现有仪器和药品:试管和胶头滴管,0.1mol?L-1 KSCN溶液、0.2mol?L-1酸性KMnO4溶液、0.1mol?L-1 KI溶液、氯水等.请你设计一个简单实验,探究A装置烧杯里完全反应后含铁可能的价态,填写下列实验报告.

(1)请简述检验它的气密性的方法.
(2)利用如图1所示装置制取气体时,可适用的反应条件和反应物状态为
某同学设计如图2所示装置,用粗铁粒与16.9%稀硝酸反应制取NO气体并探究产物中铁的价态.请回答有关问题.
(3)已知16.9%稀硝酸的密度为1.10g?cm-3,则其物质的量浓度为
(4)实验开始时,先打开止水夹a、关闭止水夹b时,A装置的干燥管中观察到的现象是
(5)现有仪器和药品:试管和胶头滴管,0.1mol?L-1 KSCN溶液、0.2mol?L-1酸性KMnO4溶液、0.1mol?L-1 KI溶液、氯水等.请你设计一个简单实验,探究A装置烧杯里完全反应后含铁可能的价态,填写下列实验报告.
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试管中滴入几滴KSCN溶液. | |
| 第二步 | 若溶液紫色褪去,则说明含有Fe2+; 若无明显变化,则说明不含Fe2+. |
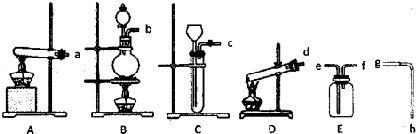
某同学设计如图1所示装置分别进行以下探究实验(夹持装置已略去,忽略滴入液体体积对气体体积的影响)
:
请回答下列问题:
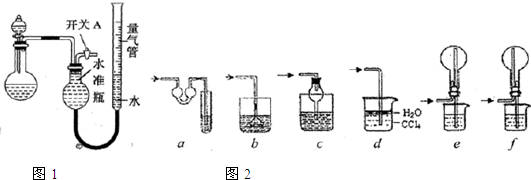
(1)实验过程中,使用分液漏斗滴加液体的操作是 .
(2)该同学认为实验I不可通过收集并测量NO气体的体积来探究铜样品的纯度,请你分析其中原因是 .
(3)实验Ⅲ烧瓶中发生反应的化学方程式是 .打开开关A,产生的气体经验纯后点燃,现象是 .
(4)实验II中量气管中的液体最好是 .(选填序号)
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理,以下各种尾气吸收装置中图2,适合于吸收NH3,而且能防止倒吸的有 .(选填序号)
(5)本实验应对量气管多次读数,读数时应注意:
①将实验装置恢复到室温,② ,③视线与凹液面最低处相平.
(6)实验Ⅳ获得以下数据(所有气体体积均己换算成标准状况):
根据上述数据,可计算出镁铝合金中铝的质量分数为 .
:
| 实验 | 药品 | 制取气体 | 量气管中液体 |
| Ⅰ | Cu、稀硝酸 | NO | H2O |
| Ⅱ | NaOH(s)、浓氨水 | NH3 | |
| Ⅲ | 电石、饱和食盐水 | C2H2 | H2O |
| Ⅳ | 镁铝合金、NaOH溶液 | H2 | H2O |

(1)实验过程中,使用分液漏斗滴加液体的操作是
(2)该同学认为实验I不可通过收集并测量NO气体的体积来探究铜样品的纯度,请你分析其中原因是
(3)实验Ⅲ烧瓶中发生反应的化学方程式是
(4)实验II中量气管中的液体最好是
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理,以下各种尾气吸收装置中图2,适合于吸收NH3,而且能防止倒吸的有
(5)本实验应对量气管多次读数,读数时应注意:
①将实验装置恢复到室温,②
(6)实验Ⅳ获得以下数据(所有气体体积均己换算成标准状况):
| 编号 | 镁铝合金质量 | 量气管第1次读数 | 量气管第2次读数 |
| ① | 1.0g | 10.0mL | 347.5mL |
| ② | 1.0g | 10.0mL | 335.0mL |
| ③ | 1.0g | 10.0mL | 344.5mL |
如图1所示是实验室中制取气体的一种简易装置.

(1)请简述检验它的气密性的方法 .
(2)利用如图1所示装置可以制取(填反应物状况及发生反应是否需要的条件) 气体.
(3)某同学设计如图2所示装置,用粗铁粒与16.9%稀硝酸反应制取NO气体并探究产物中铁的价态.请回答有关问题.已知16.9%稀硝酸的密度为1.10g/cm3,则其物质的量浓度为 (计算结果保留两位小数).用若用63%的硝酸配制16.9%稀硝酸500mL,所需的玻璃仪器有玻璃棒、烧杯和 .
(4)当打开止水夹a、关闭止水夹b时,A装置的干燥管中观察到的现象是 .B装置烧杯中液体的作用是 .当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体.
(5)已知下列反应可以发生:Fe2O3+3KNO3+4KOH
2K2FeO4+3KNO2+2H2O,而A装置中的稀硝酸即使换成浓硝酸,也不能生成+6价的铁的化合物,其原因是 .
a.HNO3的氧化性比KNO3弱
b.反应的温度不够
c.HNO3的热稳定性比KNO3差
d.FeO42-不能存在于酸性溶液中
(6)现有仪器和药品:试管和胶头滴管,0.1mol/L KSCN溶液、0.2mol/L酸性KMnO4溶液、0.1mol/L KI溶液、氯水等.请你设计一个简单实验,探究A装置烧杯里完全反应后含铁可能的价态,填写表中实验报告:

(1)请简述检验它的气密性的方法
(2)利用如图1所示装置可以制取(填反应物状况及发生反应是否需要的条件)
(3)某同学设计如图2所示装置,用粗铁粒与16.9%稀硝酸反应制取NO气体并探究产物中铁的价态.请回答有关问题.已知16.9%稀硝酸的密度为1.10g/cm3,则其物质的量浓度为
(4)当打开止水夹a、关闭止水夹b时,A装置的干燥管中观察到的现象是
(5)已知下列反应可以发生:Fe2O3+3KNO3+4KOH
| 高温 |
a.HNO3的氧化性比KNO3弱
b.反应的温度不够
c.HNO3的热稳定性比KNO3差
d.FeO42-不能存在于酸性溶液中
(6)现有仪器和药品:试管和胶头滴管,0.1mol/L KSCN溶液、0.2mol/L酸性KMnO4溶液、0.1mol/L KI溶液、氯水等.请你设计一个简单实验,探究A装置烧杯里完全反应后含铁可能的价态,填写表中实验报告:
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试 管中滴入几滴KSCN溶液. |
|
| 第二步 | 若溶液紫色褪去,则说明含有Fe2+; 若无明显变化,则说明不含Fe2+. |
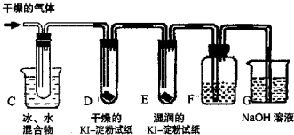
 利用如图装置,选用适当试剂,可完成实验(1)和(2),并得出相应的实验结论(见表).请填写表中的空格(从A~H中选择,填字母):
利用如图装置,选用适当试剂,可完成实验(1)和(2),并得出相应的实验结论(见表).请填写表中的空格(从A~H中选择,填字母):| 实验 | 所 用 试 剂 | 实验结论 | ||
| 甲 | 乙 | 丙 | ||
| (1) | 浓盐酸 | KI淀粉 溶液 |
||
| (2) | Cu | SO2具有 漂白性 | ||
D.MnO2粉末 E.澄清石灰水 F.NaOH溶液
G.氧化性:Cl2>I2 H.浓硫酸具有氧化性.
 实验室可用如图装置(启普发生器)制取氢气.欲使得到氢气的速率加快,下列措施可行的是( )
实验室可用如图装置(启普发生器)制取氢气.欲使得到氢气的速率加快,下列措施可行的是( )| A、将稀硫酸改用浓硫酸 | B、向稀硫酸中加入少量浓H2SO4 | C、向稀硫酸中加入Cu(NO3)2溶液 | D、给装置中发生反应的部分加热 |

 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是( )