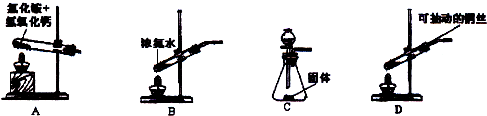
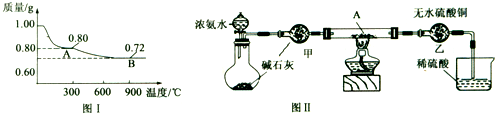
某学习小组在通过反应Na2S2O3+H2SO4═Na2SO4+S↓+SO2↑+H2O研究反应速率的影响因素后,对Na2S2O3产生了兴趣,查资料知Na2S2O3名称为硫代硫酸钠,俗称海波,可以看成是用一个S原子取代了Na2SO4中的一个O原子而形成.该实验小组运用类比学习的思想预测了Na2S2O3的某些性质,并通过实验探究验证自己的预测.
【提出假设】
(1)部分学生认为Na2S2O3与N2SO4结构相似,化学性质也相似,因此室温时Na2S2O3溶液的pH 7(填“>”、“=”或“<”).
(2)部分学生从S元素化合价推测Na2S2O3与SO2性质相似,均具有较强的 .
【实验探究】
取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写表中空格)
【实验结论】
(6)探究①: .
(7)探究②: .
【问题讨论】
(8)甲同学向“探究②”反应后的溶液中滴加硝酸银溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化.你认为该方案是否正确并说明理由 .
(9)请你重新设计二个实验方案,证明Na2S2O3被氯水氧化.你的方案是 .
0 22276 22284 22290 22294 22300 22302 22306 22312 22314 22320 22326 22330 22332 22336 22342 22344 22350 22354 22356 22360 22362 22366 22368 22370 22371 22372 22374 22375 22376 22378 22380 22384 22386 22390 22392 22396 22402 22404 22410 22414 22416 22420 22426 22432 22434 22440 22444 22446 22452 22456 22462 22470 203614
【提出假设】
(1)部分学生认为Na2S2O3与N2SO4结构相似,化学性质也相似,因此室温时Na2S2O3溶液的pH
(2)部分学生从S元素化合价推测Na2S2O3与SO2性质相似,均具有较强的
【实验探究】
取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写表中空格)
| 实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
| 探究① | (3) |
溶液pH=8 | (4) |
| 探究② | 向新制氯水(pH<2)中滴加少量Na2S2O3溶液 | 氯水颜色变浅 | (5) |
(6)探究①:
(7)探究②:
【问题讨论】
(8)甲同学向“探究②”反应后的溶液中滴加硝酸银溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化.你认为该方案是否正确并说明理由
(9)请你重新设计二个实验方案,证明Na2S2O3被氯水氧化.你的方案是
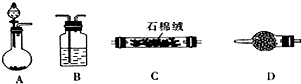
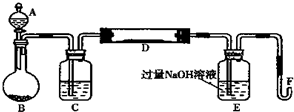
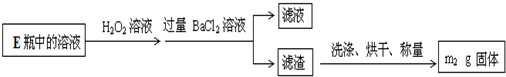
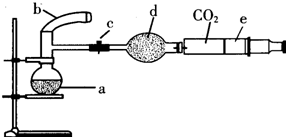 图中,a是250mL的烧瓶,其中盛有标准状况下的空气(O2占
图中,a是250mL的烧瓶,其中盛有标准状况下的空气(O2占