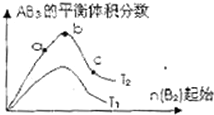
 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB2(g)化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度,n表示物质的量),据此可得出的判断结论不正确的是( )
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB2(g)化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度,n表示物质的量),据此可得出的判断结论不正确的是( )| A、达到平衡时A2的转化率大小为:b>a | B、a、b、c三点的平衡常数相同 | C、若T2>T1,则正反应一定是吸热反应 | D、b点时,平衡体系中A、B原子数之比一定是1:1 |
 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB2(g)化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度,n表示物质的量),据此可得出的判断结论不正确的是( )
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB2(g)化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度,n表示物质的量),据此可得出的判断结论不正确的是( )| A、达到平衡时A2的转化率大小为:b>a | B、a、b、c三点的平衡常数相同 | C、若T2>T1,则正反应一定是吸热反应 | D、b点时,平衡体系中A、B原子数之比一定是1:1 |