【题目】下图是物质间发生化学反应的颜色变化,下表选项物质对应正确的是

选项 | M | N | P | Q |
A | NH3·H2O | Ba(OH)2 | 铜 | KSCN |
B | Na | BaCl2 | FeO | KSCN |
C | NaOH | Ba(NO3)2 | 铁粉 | KSCN |
D | Na2O2 | MgCl2 | 锌粉 | KSCN |
A.AB.BC.CD.D
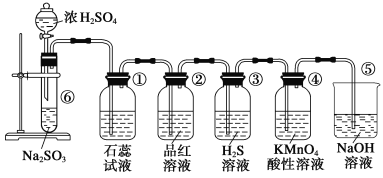
【题目】滴定实验是化学学科中重要的定量实验。请回答下列问题:
(1)酸碱中和滴定——用浓度为0.1000mol·L-1的标准盐酸滴定未知浓度的NaOH溶液,表格中记录了实验数据:
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.50 | 20.40 |
第二次 | 20.00 | 3.00 | 23.00 |
第三次 | 20.00 | 4.00 | 24.10 |
①下列操作造成测定结果偏高的是________(填选项字母)
A.滴定终点读数时,俯视滴定管刻度,其他操作正确。
B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
②该NaOH溶液的物质的量浓度为_____________mol/L。(小数点后保留四位有效数字)
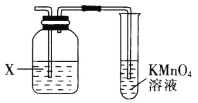
(2)氧化还原滴定——取一定量的草酸(H2C2O4)溶液置于锥形瓶中,加入适量稀硫酸,用标准酸性高锰酸钾溶液滴定。滴定时KMnO4溶液应装在______________(填“酸”或“碱”)式滴定管中,滴定终点时滴定现象是_________________________________。
(3)沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是______(填选项字母)。
难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
A.NaClB.NaBrC.NaCND.Na2CrO4