0 19546 19554 19560 19564 19570 19572 19576 19582 19584 19590 19596 19600 19602 19606 19612 19614 19620 19624 19626 19630 19632 19636 19638 19640 19641 19642 19644 19645 19646 19648 19650 19654 19656 19660 19662 19666 19672 19674 19680 19684 19686 19690 19696 19702 19704 19710 19714 19716 19722 19726 19732 19740 203614
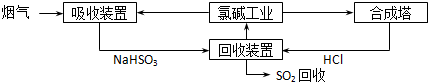
 (2012?东城区二模)某课外活动小组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”.
(2012?东城区二模)某课外活动小组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”.
 )的路线如下(A~H各表示一种有机物):
)的路线如下(A~H各表示一种有机物):


 的说法正确的是
的说法正确的是

 ”结构
”结构