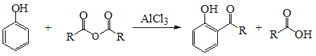
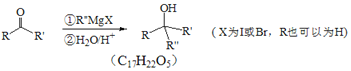
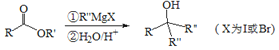
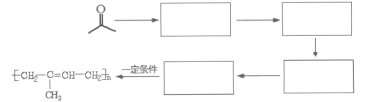
【题目】如表是A、B、C、D、E五种有机物的有关信息:
A | ①能使溴的四氯化碳溶液褪色 ②比例模型 ③能与水在一定条件下反应生成C |
B | ①由C、H两种元素组成 ②球棍模型为 |
C | ①由C、H、O三种元素组成 ②能与Na反应 ③与E反应生成相对分子质量为88的酯 |
D | ①相对分子质量比C少2 ②能由C催化氧化得到 |
E | ①由C、H、O三种元素组成 ②其水溶液能使紫色石蕊试液变红 |
回答下列问题:
(1)A~E中,属于烃的是___(填字母)。
(2)A使溴的四氯化碳溶液褪色后生成产物的结构简式为___。
(3)C催化氧化生成D的化学方程式为___。
(4)有机物B具有的性质是___(填序号)。
①无色无味的液体;②有毒:③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色。
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是___(用化学方程式说明)