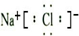0 19374 19382 19388 19392 19398 19400 19404 19410 19412 19418 19424 19428 19430 19434 19440 19442 19448 19452 19454 19458 19460 19464 19466 19468 19469 19470 19472 19473 19474 19476 19478 19482 19484 19488 19490 19494 19500 19502 19508 19512 19514 19518 19524 19530 19532 19538 19542 19544 19550 19554 19560 19568 203614
 J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.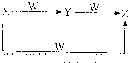 X、Y、Z、W均为短周期元素组成的物质,它们之间有如图所示转化关系:请从你所学的知述要求的X、Y、Z、W的组合.
X、Y、Z、W均为短周期元素组成的物质,它们之间有如图所示转化关系:请从你所学的知述要求的X、Y、Z、W的组合.