0 19345 19353 19359 19363 19369 19371 19375 19381 19383 19389 19395 19399 19401 19405 19411 19413 19419 19423 19425 19429 19431 19435 19437 19439 19440 19441 19443 19444 19445 19447 19449 19453 19455 19459 19461 19465 19471 19473 19479 19483 19485 19489 19495 19501 19503 19509 19513 19515 19521 19525 19531 19539 203614
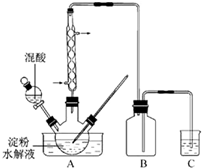 (2011?江苏)草酸是一种重要的化工产品.实验室用硝酸氧化淀粉水解液制备草酸的装置如图14所示(加热、搅拌和仪器固定装置均已略去)
(2011?江苏)草酸是一种重要的化工产品.实验室用硝酸氧化淀粉水解液制备草酸的装置如图14所示(加热、搅拌和仪器固定装置均已略去)


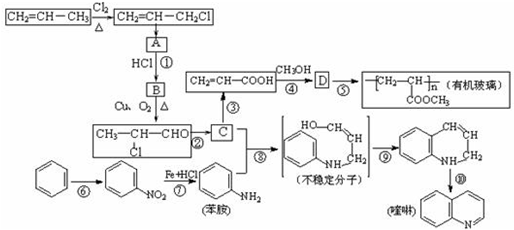
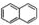 )的衍生物,且取代基都在同一个苯环上;③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氧.
)的衍生物,且取代基都在同一个苯环上;③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氧.
 ,写出以苯酚和乙醇为原料制备
,写出以苯酚和乙醇为原料制备 的合成路线流程图
的合成路线流程图