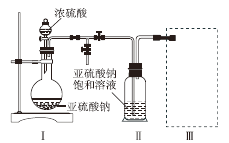
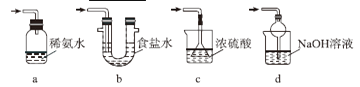
【题目】溴苯是一种化工原料,实验室用苯和液溴合成溴苯的装置示意图如下(夹持仪器已略去)。请回答以下问题。
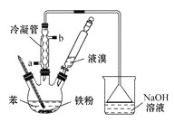
(1)制取溴苯的化学方程式是 ___________,反应过程中烧瓶内有白雾产生,是因为生成了________气体。
(2)该实验中用到冷凝管,由此猜想生成溴苯的反应属于________反应(填“放热”或“吸热”);使用冷凝管时,进水口应是______(填“a”或“b”)。
(3)该实验中将液溴全部加入苯中,充分反应后,为提纯溴苯,进行以下操作:
①将烧瓶中的液体倒入烧杯中,然后向烧杯中加入少量水,过滤,除去未反应的铁屑,过滤时必须用到的玻璃仪器是烧杯、玻璃棒、____________。
②滤液再经一系列处理,最终得到的粗溴苯中仍含有少量苯,要进一步提纯溴苯,可进行的操作是_____(填字母)。
物质 | 苯 | 溴苯 |
沸点/℃ | 80 | 156 |
水中溶解性 | 微溶 | 微溶 |
a.洗涤 b.过滤 c.蒸馏 d.结晶
【题目】甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇。
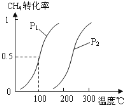
⑴①将1.0 mol CH4和2.0 mol H2O(g)通入容积100L的反应室,一定条件下发生反应:CH4(g) + H2O(g) CO(g) + 3H2(g)
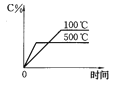
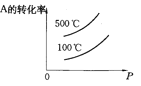
Ⅰ,CH4的转化率与温度、压强的关系如图。已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为:_____________;
②图中的压强P1_________P2(填“大于”、“小于”或“等于”),100℃时的平衡常数为:_______;
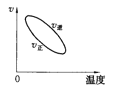
③在其它条件不变的情况下降低温度,逆反应速率将__________(填“增大”、“减小”或“不变”)。
⑵在压强为0.1 MPa条件下, 将a mol CO与 3amol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g) + 2H2(g) CH3OH(g)
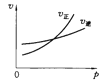
Ⅱ。①若容器容积不变,下列措施可提高甲醇产率的是:________________;
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.加入更高效的催化剂
②为了寻找合成甲醇的适宜温度和压强,某同学设计了三组实验,部分实验条件已经填在下面实验设计的表中,请帮他完成该表。
实验编号 | T(℃) | n (CO)/n(H2) | P(MPa) |
A | 150 | 1/3 | 0.1 |
B | Ⅰ | Ⅱ | 5 |
C | 350 | 1/3 | Ⅲ |
表中Ⅰ、Ⅱ、Ⅲ分别为:__________、____________、____________。