��Ŀ����
����Ŀ������������(Na2S2O5)�ǵ�ʳƷ��������֮һ��ij�о�С���������ʵ�飺
ʵ��һ�����������Ƶ���ȡ
������ͼװ��(ʵ��ǰ����װ���ڵĿ���)��ȡNa2S2O5��װ��������Na2S2O5���������������ķ�ӦΪNa2SO3 �� SO2 = Na2S2O5��
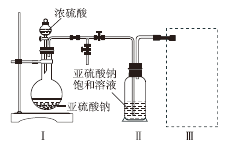
�� װ�����в�������Ļ�ѧ����ʽΪ________________________________��
�� ��ͼ��ʢװŨ����IJ���������������:__________________________;
�� װ�������ڴ���β������ѡ�õ������װ��(�г���������ȥ)Ϊ_________(�����)��

ʵ��������������Ƶ�����(Na2S2O5����ˮ������NaHSO3)
�� ֤��NaHSO3��Һ��HSO![]() �ĵ���̶ȴ���ˮ��̶ȣ��ɲ��õ�ʵ�鷽����___________(�����)��
�ĵ���̶ȴ���ˮ��̶ȣ��ɲ��õ�ʵ�鷽����___________(�����)��
a���ⶨ��Һ��pH b������Ba(OH)2��Һ c����������
d������Ʒ����Һ e������ɫʯ����ֽ���
ʵ���������Ѿ��п��������������IJⶨ
�� ���ѾƳ���Na2S2O5�������������ⶨ���Ѿ��п��������IJ�����(������SO2����)�ķ������£�(�ζ�ʱ��ӦΪSO2 �� I2 �� 2H2O = H2SO4 �� 2HI)

�������ζ������е��յ�����Ϊ______________________________________��
�ڰ���������ʵ�飬���ı�I2��Һ25.00 mL���ô�ʵ������Ʒ�п��������IJ�����(������SO2����)Ϊ____________g��L��1��
���𰸡�Na2SO3��H2SO4=Na2SO4��SO2����H2O(��Na2SO3��2H2SO4=2NaHSO4��SO2����H2O) ��Һ©�� d a��e ��Һ����ɫ���ұ��ְ���Ӳ���ɫ 0.16
��������
��1����װ�â��з����ķ�Ӧ��֪��װ�â��в�������Ϊ������������������Ũ���ᷴӦ���������ơ����������ˮ��
��2��ʢװŨ����IJ��������������ǣ���Һ©����
��3��aװ���ڵ���Ӧ�����백ˮ�У���װ��Ϊ�ܱջ�����װ����ѹǿ����������ȫ�¹ʡ�
bװ�����ն������������ϲ
cװ�ò������ն�������������ʵ�֡�
dװ��������������Һ���������Ӧ����������β�������ܷ�ֹ������
��4��HSO![]() ���ܷ�������HSO
���ܷ�������HSO![]()
![]() H++SO32-��ͬʱ�ᷢ��ˮ��HSO
H++SO32-��ͬʱ�ᷢ��ˮ��HSO![]() + H2O
+ H2O![]() H2SO3+OH-����HSO
H2SO3+OH-����HSO![]() �ĵ������HSO
�ĵ������HSO![]() ��ˮ�⣬����Һ�����ԡ�
��ˮ�⣬����Һ�����ԡ�
��5���ٵζ������е��յ�����Ϊ����Һ����ɫ���ұ��ְ���Ӳ���ɫ���ʴ�Ϊ����Һ����ɫ���ұ��ְ���Ӳ���ɫ��
�ڸ��ݷ�ӦSO2 �� I2 �� 2H2O = H2SO4 �� 2HI���㡣
��1����װ�â��з����ķ�Ӧ��֪��װ�â��в�������Ϊ������������������Ũ���ᷴӦ���������ơ����������ˮ����ѧ����ʽΪ��Na2SO3��H2SO4=Na2SO4��SO2����H2O(��Na2SO3��2H2SO4=2NaHSO4��SO2����H2O)���ʴ�Ϊ��Na2SO3��H2SO4=Na2SO4��SO2����H2O(��Na2SO3��2H2SO4=2NaHSO4��SO2����H2O)��
��2��ʢװŨ����IJ��������������ǣ���Һ©�����ʴ�Ϊ����Һ©����
��3��aװ���ڵ���Ӧ�����백ˮ�У���װ��Ϊ�ܱջ�����װ����ѹǿ����������ȫ�¹ʣ�����
bװ�����ն������������ϲ����
cװ�ò������ն�������������ʵ�֣�����
dװ��������������Һ���������Ӧ����������β�������ܷ�ֹ��������ȷ��
��ѡd��
��4��HSO![]() ���ܷ�������HSO
���ܷ�������HSO![]()
![]() H++SO32-��ͬʱ�ᷢ��ˮ��HSO
H++SO32-��ͬʱ�ᷢ��ˮ��HSO![]() + H2O
+ H2O![]() H2SO3+OH-����HSO
H2SO3+OH-����HSO![]() �ĵ������HSO
�ĵ������HSO![]() ��ˮ�⣬����Һ�����ԣ���ae��ȷ��
��ˮ�⣬����Һ�����ԣ���ae��ȷ��
��5���ٵζ������е��յ�����Ϊ����Һ����ɫ���ұ��ְ���Ӳ���ɫ���ʴ�Ϊ����Һ����ɫ���ұ��ְ���Ӳ���ɫ��
�ڸ��ݷ�ӦSO2 �� I2 �� 2H2O = H2SO4 �� 2HI������Ʒ�п��������IJ�����=(0.01mol/L��0.025L��64g/mol)/0.1L=0.16g/L���ʴ�Ϊ��0.16��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ��50mL0.50 mol��L-1��������50mL0.55 mol��L-1��NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ʵ���������±���
ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | |
���� | NaOH��Һ | �����Һ | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |

������Ϊ0.50 mol��L��1NaOH��Һ��0.50 mol��L��1HCl��Һ���ܶȶ���1g��cm��3���кͺ�������Һ�ı�����c��4.18 J��g��1������1��
��ش��������⣺��ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ���������________���ձ�����������ĭ���ϵ�������_____________�����ձ����粻��Ӳֽ�壬����õ��к�����ֵ_______(�ƫ�� ��ƫС������Ӱ�족)�����к��Ȧ�H��________(ȡС�����һλ)��
����Ŀ����ҵ�����������������Ⱦ���������·�Ӧ��
CH4(g)��2NO2(g)![]() N2(g)��CO2(g)��2H2O(g) ��H��a kJ/mol
N2(g)��CO2(g)��2H2O(g) ��H��a kJ/mol
���¶�T1��T2ʱ���ֱ�0.50 mol CH4��1.2 mol NO2�������Ϊ1 L���ܱ������У����n(CH4)��ʱ��仯�������±���
�¶� | ʱ��/min n/mol | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4) | 0.50 | 0.30 | 0.18 | ���� | 0.15 |
����˵������ȷ����
A. 10 min�ڣ�T1ʱv(CH4)T2ʱС B. �¶ȣ�T1��T2
C. ��H��a < 0 D. ƽ�ⳣ����K(T1)��K(T2)