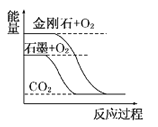
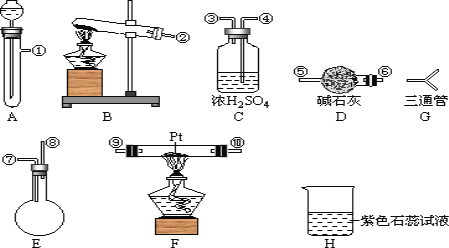
【题目】短周期五种元素A、B、C、D、E的原子序数依次增大。A、B、C的单质在常温下都呈气态,C原子最外层电子数是电子层数的3倍,C和E位于同主族。1 mol DAx与足量的A2C反应生成44.8 L(标准状况)G气体。A、B的单质依次为G、T,在密闭容器中充入一定量的G、T,一定条件下发生反应G+T→W(未配平),测得各物质的浓度如表所示。
物质 | T | G | W |
10 min时,c/(mol/L) | 0.5 | 0.8 | 0.2 |
20 min时,c/(mol/L) | 0.3 | 0.2 | 0.6 |
回答下列问题:
(1)A、B、C能组成既含离子键又含共价键的化合物,该化合物的化学式为_________。
(2)B、C、D、E的简单离子中,离子半径由大到小排序为__________(用离子符号表示)。
(3)J、L是由A、B、C、E四种元素组成的两种常见酸式盐,J、L混合可产生有刺激性气味的气体,写出这两种溶液发生反应的离子方程式__________;J、L中能使酸性高锰酸钾溶液褪色的是_______(填化学式)。
(4)B2A4C2碱性燃料电池放电效率高。该电池放电时生成B2和A2C,正极反应式为________;电池工作一段时间后,电解质溶液的pH_____(填“增大”“减小”或“不变”)。
(5)由A、B、C、D四种元素组成的单质、化合物在一定条件下的转化关系(部分条件和产物已省略)如图所示,已知M耐高温。
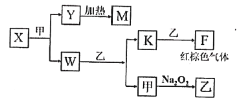
①X的电子式为______。
②已知W与乙反应生成K和甲是某重要化工生产步骤之一,提高其反应速率的方法除增大反应物浓度、增大压强外,还有______、______。
【题目】氮是动植物生长不可缺少的元素,氮在自然界中的循环对生命有重要意义。
(1)合成氨反应为N2(g)+3H2(g)![]() 2 NH3(g) H=-92.3kJ/mol,工业上为了提高H2的转化率可采取的措施是:____________________。
2 NH3(g) H=-92.3kJ/mol,工业上为了提高H2的转化率可采取的措施是:____________________。
A.使用催化剂 B.增大N2浓度 C增大压强 D.升高温度 E.及时分离生成的NH3
(2)氮的氧化物属大气污染物,为变废为宝可将NO和NO2按一定的比例通入NaOH溶液使之恰好完全被吸收生成NaNO2,写出该反应的离子方程式:_______________________________。
(3)NH3是重要的化工原料,用途广泛,如合成尿素等。合成尿素原理分两步:
CO2(g)+ 2 NH3(g)== NH2COONH4(s) H1=-159.5kJ/mol
NH2COONH4(s) == CO(NH2)2(s) + H2O(g) H2=+28.5kJ/mol
则2NH3(g)+ CO2(g)== CO(NH2)2(s) + H2O(g) H=____________kJ/mol
(4)向温度为T容积为1L的刚性密闭容器中通入1molN2和3molH2发生N2(g)+3H2(g)![]() 2NH3(g)的反应。体系总压强p与反应时间t的关系如下表:
2NH3(g)的反应。体系总压强p与反应时间t的关系如下表:
t/h | 0 | 1 | 2 | 4 | 8 | 16 |
p/Mpa | 30.0 | 28.0 | 26.5 | 25.5 | 25.0 | 25.0 |
则H2的平衡转化率α(H2)=_____(保留1位小数),平衡常数K=_____(用分数表示)。
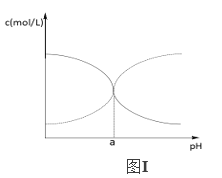
(5)现有25℃时某浓度的氯化铵溶液中NH3H2O和NH4+的浓度随pH的变化示意图如图Ⅰ所示,该温度下NH3H2O电离平衡常数为____________(用a的代数式表示)。
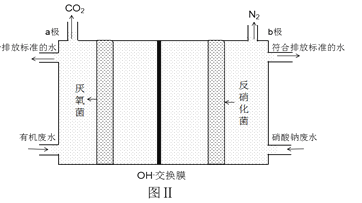
(6)利用微生物的作用将化学能转化为电能即设计成微生物电池可用于同时处理含硝酸钠和有机物的废水,使NO3- 转化为N2,装置原理如图Ⅱ(图中有机物用C6H12O6表示)。写出电极b上发生的电极反应式:_________________________________________。