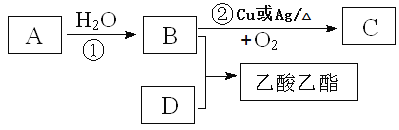
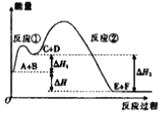
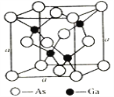
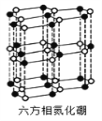
0 193655 193663 193669 193673 193679 193681 193685 193691 193693 193699 193705 193709 193711 193715 193721 193723 193729 193733 193735 193739 193741 193745 193747 193749 193750 193751 193753 193754 193755 193757 193759 193763 193765 193769 193771 193775 193781 193783 193789 193793 193795 193799 193805 193811 193813 193819 193823 193825 193831 193835 193841 193849 203614