【题目】下图装置可用于收集气体并验证其化学性质,下列对应关系完全正确的是( )
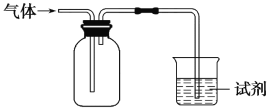
选项 | 气体 | 试剂 | 现象 | 结论 |
A | NO | 紫色石蕊溶液 | 溶液变红 | NO与水反应生成硝酸 |
B | Cl2 | 淀粉KI溶液 | 溶液变蓝 | Cl2有氧化性 |
C | SO2 | 品红溶液 | 溶液褪色 | SO2有强氧化性 |
D | NH3 | MgCl2溶液 | 产生白色沉淀 | NH3有碱性 |
A. AB. BC. CD. D
【题目】下图装置可用于收集气体并验证其化学性质,下列对应关系完全正确的是( )

选项 | 气体 | 试剂 | 现象 | 结论 |
A | NO | 紫色石蕊溶液 | 溶液变红 | NO与水反应生成硝酸 |
B | Cl2 | 淀粉KI溶液 | 溶液变蓝 | Cl2有氧化性 |
C | SO2 | 品红溶液 | 溶液褪色 | SO2有强氧化性 |
D | NH3 | MgCl2溶液 | 产生白色沉淀 | NH3有碱性 |
A. AB. BC. CD. D