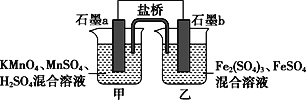
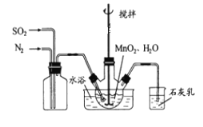
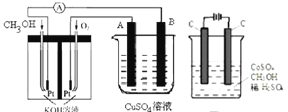
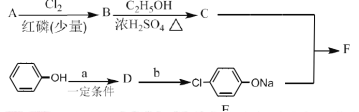
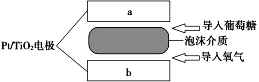
【题目】某地湖盐中含有![]() 等杂质离子,氨碱厂用该地湖盐制取烧碱。其中制得精制食盐水的过程如下:
等杂质离子,氨碱厂用该地湖盐制取烧碱。其中制得精制食盐水的过程如下:
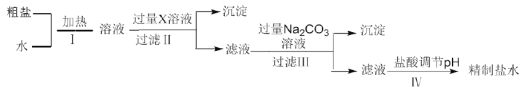
(1)过程Ⅰ中将粗盐加水溶解需要适当加热,其目的是__________。
(2)过程Ⅱ的目的是除去![]() ,加入的X溶液是__________。
,加入的X溶液是__________。
(3)下表是过程Ⅱ、Ⅲ中生成的部分沉淀及其在20℃时的溶解度[g/100g![]() ]
]
|
|
|
|
|
|
|
|
|
|
|
|
①过程Ⅲ中生成的主要沉淀除![]() 和
和![]() 外还有__________。
外还有__________。
②过程Ⅳ中调节pH时发生的主要反应的离子方程式为__________。
(4)上述精制食盐水中还含有微量的![]() ,除去这些离子及进行电解的流程如下:
,除去这些离子及进行电解的流程如下:
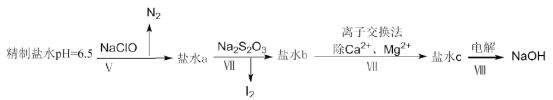
①过程Ⅴ生成![]() 的离子方程式为__________。
的离子方程式为__________。
②过程Ⅳ可以通过控制![]() 的量,将
的量,将![]() 还原为
还原为![]() ,且盐水b中含有
,且盐水b中含有![]() ,该过程中发生氧化还原反应,其中氧化剂和还原剂的物质的量之比为__________。
,该过程中发生氧化还原反应,其中氧化剂和还原剂的物质的量之比为__________。
③在过程Ⅳ中所用的![]() 俗称海波,是一种重要的化工原料。商品海波主要成分是
俗称海波,是一种重要的化工原料。商品海波主要成分是![]() .为了测定其含
.为了测定其含![]() 的纯度,称取8.00g样品,配成250mL溶液,取25.00mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为
的纯度,称取8.00g样品,配成250mL溶液,取25.00mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为![]() 的碘水滴定(发生反应
的碘水滴定(发生反应![]() ),下表记录滴定结果:
),下表记录滴定结果:
滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
第一次 | 0.30 | 29.12 |
第二次 | 0.36 | 30.56 |
第三次 | 1.10 | 29.88 |
计算样品的纯度为__________。