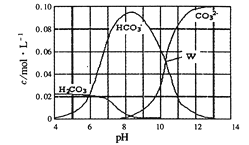
【题目】已知如表25℃时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )
CH3COOH | HClO | H2CO3 |
Ka=1.8×10﹣5 | Ka=3.0×10﹣8 | Ka1=4.4×10﹣7 Ka2=4.7×10﹣11 |

A.如图中的两种酸分别和等浓度的NaOH溶液刚好完全反应,消耗碱的体积相等
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO﹣+CO2+H2O═2HClO+CO32﹣
C.a、b、c三点所示溶液中水的电离程度c>a>b
D.图象中,Ⅰ表示CH3COOH,Ⅱ表示HClO,且溶液导电性:c>b>a
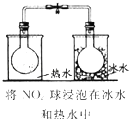
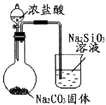
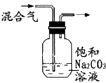
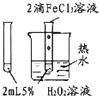
【题目】下列图中的实验方案,能达到实验目的是( )
A | B | C | D | |
实验方案 |
|
|
|
|
实验目的 | 探究温度对平衡的影响 | 比较HCl、H2CO2和 | 除去CO2气体中混有的SO2 | 验证FeCl3对H2O2分解反应有催化作用 |
A.A
B.B
C.C
D.D
【题目】某些化学问题可用相似的示意图来表示。下列说法不正确的是

选项 | 横坐标 | 纵坐标 | 研究对象 |
A | 反应过程 | 能量 | NH4Cl和Ba(OH)2 ·8H2O反应 |
B | 反应温度 | 反应速率 | 酶催化反应 |
C | HCl溶液体积 | 沉淀质量 | 0.1 mol·L-1盐酸滴加到同浓度AgNO3溶液中 |
D | 反应时间 | 溶液温度 | 足量未打磨的镁条放在1mol·L-1H2SO4溶液中 |
A. A B. B C. C D. D