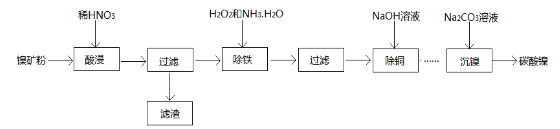
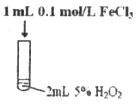
【题目】某研究小组设计了如下实验,探究常温下催化剂对过氧化氢分解反应的影响。
Ⅰ | Ⅱ | Ⅲ | |
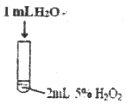
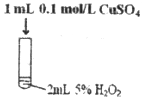
实验操作 示意图 |
|
|
|
实验现象 | 有极少量气泡产生 | 产生气泡速率略有加快 | 产生气泡速率明显加快 |
(1)实验Ⅰ的作用是_______________。
(2)实验Ⅲ中反应的化学方程式为_______________。
(3)根据实验Ⅰ~Ⅲ中现象的不同,可以得出的结论是:
①使用合适的催化剂,可提高双氧水分解的反应速率;
②_______________。
(4)在一定温度下,10 mL 0.40 mol/L,H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表所示:
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
0~6 min,以H2O2的浓度变化表示的反应速率为v(H2O2)=_________mol/(L·min)。(计算结果精确到0.001)
【题目】700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法正确的是
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法正确的是
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 1.2 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
A. 反应在t1min内的平均速率为v(H2)=0.40/t1mol/(L·min)
B. 温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
C. 保持其他条件不变,起始时向容器中充入0.60molCO和1.20molH2,到达平衡时,n(CO2)=0.40mol
D. 保持其他条件不变,向平衡体系中再通入0.20molCO,与原平衡相比,达到新平衡时CO转化率减小,H2O的体积分数也减小