题目内容
【题目】已知常温下CH3COOH和NH3·H2O的电离平衡常数分别为Ka、Kb。若在常温下向0.1mol/L的醋酸溶液中逐滴加入相同浓度的氨水直至完全过量,则下列说法正确的是
A. 加入氨水的过程中,溶液的导电性一直不断增强
B. CH3COONH4在水溶液中的水解平衡常数Kh=Kw/(Ka+Kb)
C. 若Ka≈Kb,当加入等体积的氨水时,溶液基本呈中性
D. 该等式在滴加过程中始终成立c(CH3COO-)+c(CH3COOH)=c(NH4+)+c(NH3·H2O)
【答案】C
【解析】CH3COOH和NH3·H2O都是弱电解质,加入氨水的过程中生成强电解质醋酸铵,氨水过量后,氨水稀释醋酸铵溶液,导电性降低,所以溶液的导电性先增强再降低,故A错误;CH3COONH4在水溶液中的水解的离子方程式是CH3COO-+ NH4++H2O![]() CH3COOH+ NH3·H2O,Kb=
CH3COOH+ NH3·H2O,Kb= ,Kh=Kw/(Ka×Kb),故B错误;若Ka≈Kb,当加入等体积的氨水时,CH3COO-、NH4+水解程度相同,溶液基本呈中性,故C正确;根据元素守恒,当加入氨水体积小于醋酸时c(CH3COO-)+c(CH3COOH)>c(NH4+)+c(NH3·H2O);时当加入等体积的氨水时,c(CH3COO-)+c(CH3COOH)=c(NH4+)+c(NH3·H2O);当加入氨水体积小于醋酸时c(CH3COO-)+c(CH3COOH)<c(NH4+)+c(NH3·H2O);故D错误。
,Kh=Kw/(Ka×Kb),故B错误;若Ka≈Kb,当加入等体积的氨水时,CH3COO-、NH4+水解程度相同,溶液基本呈中性,故C正确;根据元素守恒,当加入氨水体积小于醋酸时c(CH3COO-)+c(CH3COOH)>c(NH4+)+c(NH3·H2O);时当加入等体积的氨水时,c(CH3COO-)+c(CH3COOH)=c(NH4+)+c(NH3·H2O);当加入氨水体积小于醋酸时c(CH3COO-)+c(CH3COOH)<c(NH4+)+c(NH3·H2O);故D错误。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】汽车尾气中含有CO、NO等有害气体。
(1)汽车尾气中NO生成过程的能量变化示意图如下:
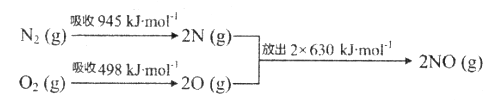
该条件下,1mol N2和1molO2完全反应生成NO,会_______________(填“吸收”或“放出”)________kJ能量。
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如下图所示:
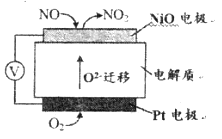
①NiO电极上发生的是_______________反应(填“氧化”或“还原”)。
②外电路中,电子的流动方向是从_______电极流向______电极(填“NiO”或“Pt”);Pt电极上的电极反应式为_______________。
(3)一种新型催化剂能使NO和CO发生反应:2NO+2CO ![]() 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
实验 编号 | t(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
Ⅱ | 280 | 1.20×10-3 | B | 124 |
Ⅲ | 350 | A | 5.80×10-3 | 82 |
①请把表中数据补充完整:A_______________;B_______________。
②能验证温度对化学反应速率影响规律的是实验_______________(填实验序号)。
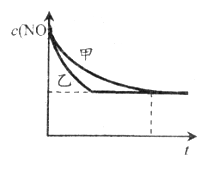
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如下图所示,其中表示实验Ⅱ的是曲线_________(填“甲”或“乙”)。
【题目】现有反应:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的 ( )
实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
V/mL | c/(molL﹣1) | V/mL | c/(molL﹣1) | V/mL | ||
A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
A.A
B.B
C.C
D.D