题目内容
【题目】700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法正确的是
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法正确的是
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 1.2 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
A. 反应在t1min内的平均速率为v(H2)=0.40/t1mol/(L·min)
B. 温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
C. 保持其他条件不变,起始时向容器中充入0.60molCO和1.20molH2,到达平衡时,n(CO2)=0.40mol
D. 保持其他条件不变,向平衡体系中再通入0.20molCO,与原平衡相比,达到新平衡时CO转化率减小,H2O的体积分数也减小
【答案】CD
【解析】t1min内消耗0.4molCO,生成氢气0.4mol,v(H2)= ![]() 0.20/t1mol/(L·min),故A错误;t1min内消耗0.4molCO,消耗0.4mol H2O,所以t1min时水的物质的量是0.2mol,t1min时水的物质的量是0.2mol,可知t2min时反应达到平衡,
0.20/t1mol/(L·min),故A错误;t1min内消耗0.4molCO,消耗0.4mol H2O,所以t1min时水的物质的量是0.2mol,t1min时水的物质的量是0.2mol,可知t2min时反应达到平衡,
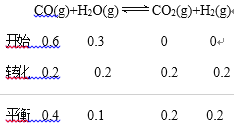
K=![]() ,温度升至800℃,上述反应平衡常数为0.64,说明平衡逆向移动,正反应为放热反应,故B错误;保持其他条件不变,起始时向容器中充入0.60molCO和1.20molH2
,温度升至800℃,上述反应平衡常数为0.64,说明平衡逆向移动,正反应为放热反应,故B错误;保持其他条件不变,起始时向容器中充入0.60molCO和1.20molH2
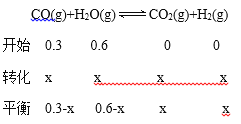
![]() ,则x=0.2mol/L,所以n(CO2)=0.40mol,故C正确;
,则x=0.2mol/L,所以n(CO2)=0.40mol,故C正确;
保持其他条件不变,向平衡体系中再通入0.20molCO,平衡正向移动,达到新平衡时CO转化率减小,H2O的体积分数也减小,故D正确。

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目