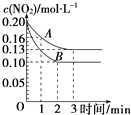
【题目】1000ml某无色待测液中除含有0.2molL﹣1的Na+外,还可能含有下列离子中的一种或多种:
阳离子 | K+、NH4+、Fe3+、Ba2+ |
阴离子 | Cl﹣、CO32﹣、HCO3﹣、SO42﹣ |
现进行如下实验操作(所加试剂均过量):(已知:NH4++OH﹣(浓)=NH3↑+H2O)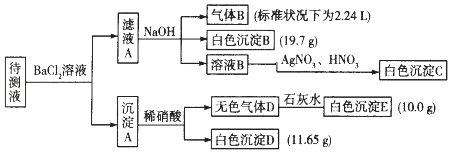
(1)原溶液中肯定存在的离子是(除Na+) , 肯定不存在的离子是 .
(2)写出生成白色沉淀B的离子方程式: . 写出沉淀A溶于稀硝酸的离子方程式: .
(3)将滤液A和沉淀A分开的操作是过滤,洗涤.洗涤的操作是 .
【题目】电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如表所示:
化学式 | HF | H2CO3 | HClO |
电离平衡常数(Ka) | 7.2×10﹣4 | K1=4.4×10﹣7 | 3.0×10﹣8 |
(1)将浓度为0.1molL﹣1 HF溶液加水稀释一倍(假设温度不变),下列各量增大的是 .
A.c(H+)
B.c(H+)c(OH﹣)
C.![]()
D.![]()
(2)25℃时,在20mL 0.1molL﹣1氢氟酸中加入V mL 0.1molL﹣1 NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是 . 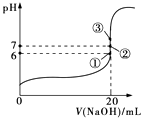
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中c(F﹣)﹣c(Na+)=9.9×10﹣7 molL﹣1
C.②点时,溶液中的c(F﹣)=c(Na+)
D.③点时V=20mL,此时溶液中c(F﹣)<c(Na+)=0.1molL﹣1
(3)物质的量浓度均为0.1molL﹣1的下列四种溶液:①Na2CO3溶液;②NaHCO3溶液;③NaF溶液;④NaClO溶液.依据数据判断pH由大到小的顺序是 .
(4)Na2CO3溶液显碱性是因为CO32﹣水解的缘故,请设计简单的实验事实证明之 .
(5)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H﹣O﹣F.HFO与水反应得到HF和化合物A,每生成1mol HF转移mol电子.