【题目】有部分元素的性质与原子(或分子)结构如下表,根据信息回答下列问题:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 其气态氢化物与最高价氧化物对应的水化物能起化合反应 |
Y | M层比K层少1个电子 |
Z | 第三周期元素的简单离子中半径最小 |
W | L层电子数是K层和M层电子数之和 |
(1)写出元素X形成的单质的电子式:__________;
(2)元素Y与元素Z相比,金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________(填序号)。
a.Y单质的熔点比Z单质低 b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈 d.Y最高价氧化物对应的水化物的碱性比Z强
(3)元素T与元素W相比,非金属性较强的是________(用元素符号表示),写出一个能表示T、W非金属性强弱关系的化学反应方程式 。
(4)写出T与Y形成的化合物的化学式__________,__________。
(5)元素T和氢元素以原子个数比1∶1化合形成化合物P,元素X与氢元素以原子个数比1∶2化合形成常用作火箭燃料的化合物Q,P与Q发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式:_____________________________。
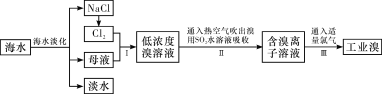
【题目】工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:

(1)金属M为 。
(2)加入H2O2的作用是(用离子方程式表示) ,加入氨水的作用是 。
(3)CoC2O4﹒2H2O高温焙烧的化学方程式为 。
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表。操作2中,蒸发浓缩后必须趁热过滤,其目的是 ,90℃时Ksp(Li2CO3)的值为 。
温度/℃ | 10 | 30 | 60 | 90 |
浓度/molL-1 | 0.21 | 0.17 | 0.14 | 0.10 |
【题目】某市场销售的某种食用精制盐包装袋上有如下说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50 mg/kg |
分装日期 | |
分装企业 |
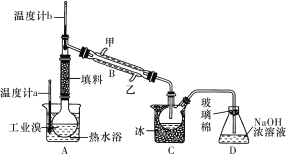
(1)I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是:________________________________________________。
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是____________________________________________。
(2)已知:I2+2S2O32-===2I-+S4O62-。
某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol·L-1的Na2S2O3溶液10.0 mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是________________________。
②b中反应所产生的I2的物质的量是______________mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)____________mg/kg。