10.实验室中某溶液含有Ag+、Cu2+、Ba2+,若依次加入试剂使三种离子分别沉淀出来,过滤得到相应的沉淀,则加入试剂的顺序为( )
| A. | NaOH、Na2SO4、NaCl | B. | NaCl、Na2SO4、NaOH | ||
| C. | NaOH、NaCl、Na2SO4 | D. | Na2SO4、NaOH、NaCl |
9.离子方程式mFe2++4H++O2=mFe3++2H2O,则m为( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
8.在下列反应中,HCl既表现酸性又表现氧化性的是( )
| A. | CaCO3+2HCl=CaCl2+H2O+CO2↑ | |
| B. | Fe+2HCl═FeCl2+H2↑ | |
| C. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑ | |
| D. | NaOH+HCl=NaCl+H2O |
7.已知在溶液中可发生如下反应:Br2+2Fe2+═2Fe3++2Br-,Cl2+2Br-═Br2+2Cl-.由此推断Br2、Cl2、Fe3+的氧化性由强到弱的顺序是( )
| A. | Cl2、Br2、Fe3+ | B. | Br2、Cl2、Fe3+ | C. | Fe3+、Cl2、Br2 | D. | Cl2、Fe3+、Br2 |
6.下列关于电解质的说法中正确的是( )
| A. | 纯水的导电性很差,所以水不是电解质 | |
| B. | SO2水溶液的导电性很好,所以SO2是电解质 | |
| C. | 熔融状态时铜的导电性很好,所以铜是电解质 | |
| D. | 硝酸钾在水中和熔融状态时都能导电,所以硝酸钾是电解质 |
5.下列叙述正确的是( )
①足量锌跟一定量的稀硫酸反应时,加入少量硫酸铜溶液能加快反应速率且不影响产气量
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,可以电解熔融态的AlCl3
⑤钢铁表面常易锈蚀生成Fe2O3•nH2O.
①足量锌跟一定量的稀硫酸反应时,加入少量硫酸铜溶液能加快反应速率且不影响产气量
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,可以电解熔融态的AlCl3
⑤钢铁表面常易锈蚀生成Fe2O3•nH2O.
| A. | ②④ | B. | ①③⑤ | C. | ①②③⑤ | D. | ①②③④⑤ |
4.铜锌原电池(如图)工作时,下列叙述正确的是( )
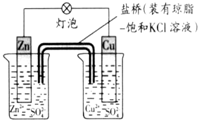

| A. | 正极反应为:Zn-2e-=Zn2+ | B. | Cu为负极,发生还原反应 | ||
| C. | 盐桥中的K+移向ZnSO4溶液 | D. | 在外电路中,电子从负极流向正极 |
3.下列说法正确的是( )
| A. | 酿酒过程中,葡萄糖可通过水解反应生成酒精 | |
| B. | 工业上利用油脂生产肥皂、用淀粉酿酒、用纤维素生产酒精 | |
| C. | 酸性高锰酸钾紫色溶液中加入植物油充分振荡后,溶液颜色不会因反应褪去 | |
| D. | 蛋白质和油脂在发生腐败变质时,均会产生含NH3的刺激性气味 |
2.高氯酸铜[Cu(ClO4)2•6H2O]易溶于水,120℃开始分解,常用于生产电极和作催化剂等.可由氯化铜通过下列反应制备:2CuCl2+2Na2CO3+H2O═Cu2(OH)2CO3↓+CO2↑+4NaCl;Cu2(OH)2CO3+4HClO4+9H2O═2Cu(ClO4)2•6H2O+CO2↑.HClO4是易挥发的发烟液体,温度高于130℃易爆炸.下表列出相应金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1mol•L-1):
(1)将CuCl2和Na2CO3用研钵分别研细,加入适量的沸水,搅拌,加热成蓝棕色溶液.静置、冷却、过滤、洗涤得蓝色Cu2(OH)2CO3沉淀.
①把反应物研细的目的是增大反应物之间的接触面积,使反应速率增大.
②检验沉淀是否洗涤干净,应选用试剂是HNO3和AgNO3溶液.
(2)向Cu2(OH)2CO3沉淀中滴加稍过量的HClO4小心搅拌,适度加热后得到蓝色Cu(ClO4)2溶液同时会产生大量的白雾.
①大量的白雾的成分是HClO4(填化学式).
②适度加热但温度不能过高的原因是防止HClO4、Cu(ClO4)2分解.
(3)25℃时,若调节溶液pH=3,则溶液中的Fe3+的物质的量浓度为2.64×10-6mol•L-1.(已知25℃时,Fe(OH)3的Ksp=2.64×10-39)
(4)某研究小组欲用粗CuCl2固体(含Fe2+)制备纯净的无水氯化铜固体.请补充完整由粗CuCl2固体制备纯净的无水氯化铜固体的实验步骤(可选用的试剂:蒸馏水、稀盐酸、双氧水溶液和氨水):①将粗CuCl2固体溶于蒸馏水,滴入少量的稀盐酸;②加入适量双氧水溶液并充分混合,再加入适量氨水调节溶液pH至3.2~4.7,过滤;③将滤液将滤液加热浓缩,冷却结晶,过滤、(冰水)洗涤,干燥,得到CuCl2•2H2O晶体;④将将 CuCl2•2H2O晶体在HCl气氛中加热至质量不再变化为止,得到无水氯化铜固体.
0 173809 173817 173823 173827 173833 173835 173839 173845 173847 173853 173859 173863 173865 173869 173875 173877 173883 173887 173889 173893 173895 173899 173901 173903 173904 173905 173907 173908 173909 173911 173913 173917 173919 173923 173925 173929 173935 173937 173943 173947 173949 173953 173959 173965 173967 173973 173977 173979 173985 173989 173995 174003 203614
| 金属离子 | 开始沉淀 | 沉淀完全 |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Cu2+ | 4.7 | 6.7 |
①把反应物研细的目的是增大反应物之间的接触面积,使反应速率增大.
②检验沉淀是否洗涤干净,应选用试剂是HNO3和AgNO3溶液.
(2)向Cu2(OH)2CO3沉淀中滴加稍过量的HClO4小心搅拌,适度加热后得到蓝色Cu(ClO4)2溶液同时会产生大量的白雾.
①大量的白雾的成分是HClO4(填化学式).
②适度加热但温度不能过高的原因是防止HClO4、Cu(ClO4)2分解.
(3)25℃时,若调节溶液pH=3,则溶液中的Fe3+的物质的量浓度为2.64×10-6mol•L-1.(已知25℃时,Fe(OH)3的Ksp=2.64×10-39)
(4)某研究小组欲用粗CuCl2固体(含Fe2+)制备纯净的无水氯化铜固体.请补充完整由粗CuCl2固体制备纯净的无水氯化铜固体的实验步骤(可选用的试剂:蒸馏水、稀盐酸、双氧水溶液和氨水):①将粗CuCl2固体溶于蒸馏水,滴入少量的稀盐酸;②加入适量双氧水溶液并充分混合,再加入适量氨水调节溶液pH至3.2~4.7,过滤;③将滤液将滤液加热浓缩,冷却结晶,过滤、(冰水)洗涤,干燥,得到CuCl2•2H2O晶体;④将将 CuCl2•2H2O晶体在HCl气氛中加热至质量不再变化为止,得到无水氯化铜固体.
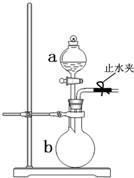 如图所示装置是实验室常用的气体制取装置.据图回答下列问题:
如图所示装置是实验室常用的气体制取装置.据图回答下列问题: