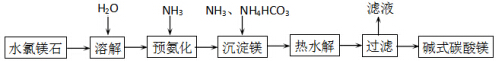
1.利用如图装置,完成很多电化学实验.下列有关此装置的叙述中,正确的是( )


| A. | 若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阴极的阳极保护法 | |
| B. | 若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动 | |
| C. | 若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阴离子向铁电极移动 | |
| D. | 若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小 |
18.下列说法或表示方法正确的是( )
| A. | 由C(石墨)=C(金刚石)△H=+11.9 kJ/mol,可知金刚石比石墨稳定 | |
| B. | 等质量的硫蒸气和硫固体分别在氧气中完全燃烧,后者放出的热量多 | |
| C. | 水力(水能)按不同的分类可看成可再生能源和一级能源 | |
| D. | 可表示氢气燃烧热的热化学方程式为H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8 kJ/mol |
17.下列除杂方法正确的是( )
①除去乙烷中少量乙烯:通入足量H2,加入催化剂反应
②除去乙酸乙酯中的少量的乙酸:用足量饱和碳酸钠溶液洗涤,分液
③除去苯中少量的苯酚:滴入足量溴水,过滤
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
⑤除去苯中少量的甲苯:先加足量酸性KMnO4溶液振荡后加足量的NaOH溶液,分液.
①除去乙烷中少量乙烯:通入足量H2,加入催化剂反应
②除去乙酸乙酯中的少量的乙酸:用足量饱和碳酸钠溶液洗涤,分液
③除去苯中少量的苯酚:滴入足量溴水,过滤
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
⑤除去苯中少量的甲苯:先加足量酸性KMnO4溶液振荡后加足量的NaOH溶液,分液.
| A. | ①②③ | B. | ③④⑤ | C. | ②④⑤ | D. | ②③④ |
14.某可逆反应:A(g)+3B(g)?2C(g);△H<0.有甲乙两个容积为0.5L的密闭容器,向甲容器中加入1molA的和3molB在一定条件下达到平衡时放出热量为Q1 kJ;在相同条件下,向乙容器中加入2mol C达到平衡时吸收热量为Q2kJ;已知Q2=3Q1.下列叙述不正确的是( )
0 173764 173772 173778 173782 173788 173790 173794 173800 173802 173808 173814 173818 173820 173824 173830 173832 173838 173842 173844 173848 173850 173854 173856 173858 173859 173860 173862 173863 173864 173866 173868 173872 173874 173878 173880 173884 173890 173892 173898 173902 173904 173908 173914 173920 173922 173928 173932 173934 173940 173944 173950 173958 203614
| A. | 乙中C的转化率为75% | |
| B. | 反应达到平衡前,甲中始终有v正大于v逆,乙中始终有v正小于v逆 | |
| C. | 在该条件下,反应 2C(g)?A(g)+3B(g)的平衡常数为27×1.54(mol/L)2 | |
| D. | 乙中的热化学方程式为2C(g)?A(g)+3B(g);△H=+Q2kJ/mol |
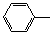 ):
):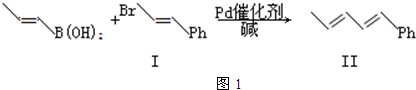
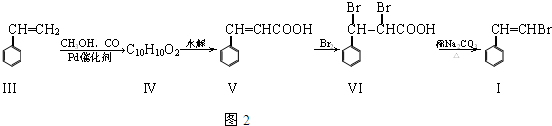
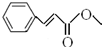 ;
; .
.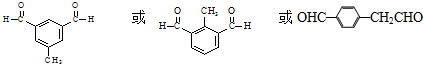 .
.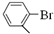 )与化合物【
)与化合物【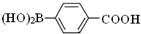 】也能发生类似反应①的偶联反应,写出产物的结构简式
】也能发生类似反应①的偶联反应,写出产物的结构简式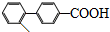 .
.
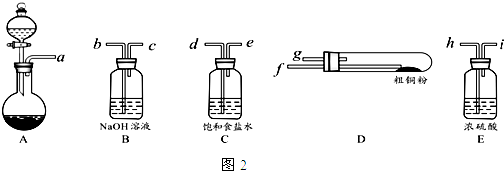
 与
与 互为同分异构体
互为同分异构体 与
与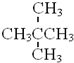 属于同系物
属于同系物 与
与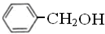 既不是同系物也不是同分异构体.
既不是同系物也不是同分异构体.

 .
.