��Ŀ����
3��Suzukiż����Ӧ���л��ϳ����й㷺Ӧ�ã���Ӧ����ͼ1��Ph-��������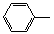 ����
����
������I������ͼ2;���ϳɣ�
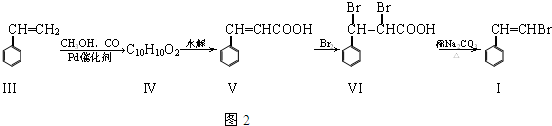
��1��������V�ķ���ʽΪC9H8O2��1mol������I���ɸ�4mol������Ӧ��
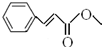
��2���ü���ʽ��ʾ������IV�Ľṹ
 ��
��������Vת��Ϊ������VI�ķ�Ӧ����Ϊ�ӳɷ�Ӧ��
��3��д��������VI��NaOH��Һ�й��ȵķ�Ӧ����ʽ
 ��
����4����֪��������ǻ�����V��ͬ���칹�壬�䱽����һ�������2�֣���1mol��������������Һ��Ӧ����4mol Ag��д��������������нṹ��ʽ
 ��
����5�������
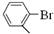 ���뻯���
���뻯��� ��Ҳ�ܷ������Ʒ�Ӧ�ٵ�ż����Ӧ��д������Ľṹ��ʽ
��Ҳ�ܷ������Ʒ�Ӧ�ٵ�ż����Ӧ��д������Ľṹ��ʽ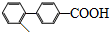 ��
��
���� ��1�����ݢ��Ľṹ��ʽȷ�������ʽ�����ݢ�IJ����Ͷȿ�ȷ�����������ʵ�����
��2��������IVˮ��õ�V����IV�д������������IV����ʽ��V�Ľṹ��֪��IVˮ��õ�V�ͼ״�����V������̼̼˫����̼̼���������Է����ӳɷ�Ӧ��
��3����������д����Ȼ�����ԭ�ӣ������������������Ʒ�Ӧ�������к͡�ˮ�ⷴӦ��
��4��1mol��������������Һ��Ӧ����4mol Ag���ʣ�˵����������д���2��ȩ�����˴Ź����������� 4�ַ壬�����֮��Ϊ3��2��2��1��˵����4��Hԭ�ӣ�˵��2��ȩ�����ڼ�λ������2��ȩ�����м䣻
��5���۲췴Ӧ�ٵ��ص㣬2�����ʷ����� Brԭ�ӡ�-B��OH��2ͬʱȥ���������µĻ����������ɣ�
��� �⣺��1���ɻ�������Ľṹ��ʽ�ж������ʽΪC8H7Br��ÿ��������I��������һ��������һ��̼̼˫��������1mol������I���ɸ�4mol������Ӧ��
�ʴ�Ϊ��C9H8O2��4��
��2��������IVˮ��õ�V����IV�д������������IV����ʽ��V�Ľṹ��֪��IVˮ��õ�V�ͼ״������Ի�����IV�Ľṹ��ʽΪ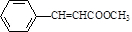 ������ʽΪ
������ʽΪ ����V������̼̼˫����̼̼���������Է����ӳɷ�Ӧ��
����V������̼̼˫����̼̼���������Է����ӳɷ�Ӧ��
�ʴ�Ϊ�� ���ӳɷ�Ӧ��
���ӳɷ�Ӧ��
��3����������д����Ȼ�����ԭ�ӣ������������������Ʒ�Ӧ�������к͡�ˮ�ⷴӦ����ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��4��1mol��������������Һ��Ӧ����4mol Ag���ʣ�˵����������д���2��ȩ�����䱽����һ�������2�֣����Է��������Ļ��������3��Ϊ ��
��
�ʴ�Ϊ�� ��
��
��5���۲췴Ӧ�ٵ��ص㣬2�����ʷ����� Brԭ�ӡ�-B��OH��2ͬʱȥ���������µĻ����������ɣ����Բ���Ľṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶ���ϳɡ��л���Ӧ���͡�ͬ���칹����д���л���Ӧ����ʽ��д�ȣ�ע������л���Ľṹ���������Ҫѧ���߱���ʵ�Ļ������������֪ʶ���������Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д���1����λ�ڵ�������VIB�壮�������ڵ���һ����ͬ��Ԫ�صķ���ΪCr����Ԫ�ػ�̬ԭ�ӵĵ�������Ų����ܼ�Ϊ3d�����ܼ����ܵĵ�����Ϊ5��
��2��̼�����й����������
| Ԫ�� | ԭ�Ӱ뾶 | �縺�� | ��һ������ |
| C | 67pm | 2.55 | 1125.8kJ/mol |
| S | 88pm | 2.58 | 1036.7kJ/mol |
��д����֤���ý��۵Ļ�ѧ����ʽH2SO4+Na2CO3=Na2SO4+CO2��+H2O��
��3���Ӳ�ͬ�Ƕȹ۲�MoS2�ľ���ṹ��ͼ1��2������MoS2�ľ���ṹ�ش�
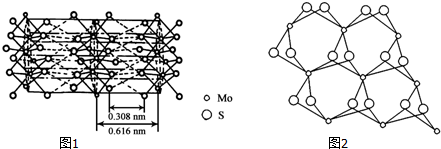
�������λ��Ϊ6��
��Mo��S֮��Ļ�ѧ��ΪAC������ţ���
A�����Լ� B���Ǽ��Լ� C����λ�� D�������� E�����»���
�ۻ����������ӵ������ܷdz����죬��ԭ����MoS2���в�״�ṹ��Mo��Sͬ����Թ��ۼ���ϣ������֮��ͨ�����»�����ϣ��������ò����������Ի�����
��4������̼�ڸ����·�Ӧ�ɵõ����ɰ��SiC������ṹ����ʯ�ṹ���ƣ��������ʯ������һ���Cԭ�ӻ���Siԭ����ͬ��ԭ�Ӳ��ɼ�����õĽ��ɰ��SiC���ṹ�����������һ����ԭ��Ϊ���ģ���SiC�����й�ԭ�����������̼ԭ�ӵ��������Ϊd�������ԭ�Ӵν��ĵڶ�����12��ԭ�ӣ���������ԭ�ӵľ�����$\frac{2\sqrt{6}}{3}$d��
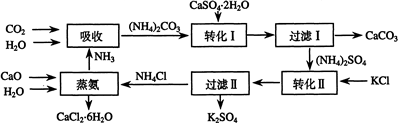
��1�������������õ�ԭ�ϳ�CaSO4•2H2O��KCl�⣬����ҪCaCO3������CaO����NH3��H2O��ԭ��
��2��д��ʯ������Һ�м���̼�����Һ������Ӧ�����ӷ���ʽ��
CaSO4+CO32-=CaCO3+SO42-
��3�����ˢ�������ù����У���CaCO3�����CaSO4���ѧʽ�������ʣ��ù������������ˮ���ԭ�ϣ�
��4�����ˢ����������Һ�ǣ�NH4��2SO4��Һ��������Һ�к���CO32-�ķ����ǣ�ȡ������Һ���μ�ϡ���ᣬ�������ݲ�������CO32-��
��֮����CO32-��
��5����֪��ͬ�¶���K2SO4��100gˮ�дﵽ����ʱ�ܽ���������
| �¶ȣ��棩 | 0 | 20 | 60 |
| K2SO4�ܽ������g�� | 7.4 | 11.1 | 18.2 |
��6���Ȼ��ƽᾧˮ���CaCl2•6H2O����Ŀǰ���õ������Ȳ��ϣ�ѡ���������Ad
A���۵�ϵͣ�29���ۻ��� b���ܵ��� c�������� d����
��7����������������������ɫ��ѧ������ǣ�̼���������ˮ��ԭ�ϡ�����ƺ��Ȼ���ת��Ϊ����غ��Ȼ��ơ����ڹ�����ѭ��ʹ�õ�
ԭ�������ʸߣ�û���к������ŷŵ������У�
| A�� | ��ԭ�ԣ�X-��Y- | |
| B�� | ��X-��Y-��Z-��W- �� Z- �Ļ�ԭ����ǿ | |
| C�� | �����ԣ�Z2��W2 | |
| D�� | ��Ӧ2Z-+Y2=2Y-+Z2���Է��� |
| A�� | ��C��ʯī��=C�����ʯ����H=+11.9 kJ/mol����֪���ʯ��ʯī�ȶ� | |
| B�� | ���������������������ֱ�����������ȫȼ�գ����߷ų��������� | |
| C�� | ˮ����ˮ�ܣ�����ͬ�ķ���ɿ��ɿ�������Դ��һ����Դ | |
| D�� | �ɱ�ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪH2��g��+$\frac{1}{2}$O2��g��=H2O��g����H=-241.8 kJ/mol |
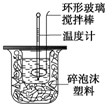 ������ͼװ�òⶨ�к��ȵ�ʵ�鲽�����£�
������ͼװ�òⶨ�к��ȵ�ʵ�鲽�����£�������Ͳ��ȡ50mL 0.25mol/L���ᵹ��С�ձ��У���������¶ȣ�
������һ��Ͳ��ȡ50mL 0.55mol/L NaOH��Һ��������һ�¶ȼƲ�����¶ȣ�
�۽�NaOH��Һ����С�ձ��У��跨ʹ֮��Ͼ��ȣ�������Һ����¶ȣ�
�ش��������⣺
��1��д��ϡ�����ϡ����������Һ��Ӧ��ʾ�к��ȵ��Ȼ�ѧ����ʽ���к�����ֵΪ57.3kJ/mol����$\frac{1}{2}$H2SO4��aq��+NaOH��aq���T$\frac{1}{2}$Na2SO4��aq��+H2O��l����H=-57.3kJ•mol-1��
��2������NaOH��Һ����ȷ������C��������ѡ������
A���ز������������롡B���������������� C��һ��Ѹ�ٵ���
��3��ʹ������NaOH��Һ��Ͼ��ȵ���ȷ������D ��������ѡ������
A�����¶ȼ�С�Ľ��� B���ҿ�ӲֽƬ�ò���������
C����������ձ� D���������¶ȼ��ϵĻ��β���������ؽ���
��4��ʵ���������±���
������д�±��еĿհף�
| �¶� ʵ������� | ��ʼ�� ��t1�� | ��ֹ�¶�t2/�� | �¶Ȳ�ƽ��ֵ��t2-t1��/�� | ||
| H2SO4 | NaOH | ƽ��ֵ | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
�� ȡС�����һλ����
������ʵ����ֵ�����57.3kJ/mol��ƫ�����ƫ���ԭ������ǣ�����ĸ��abcd��
a��ʵ��װ�ñ��¡�����Ч����
b����ȡNaOH��Һ�����ʱ���Ӷ���
c���ֶ�ΰ�NaOH��Һ����ʢ�������С�ձ���
d�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶�
��5����֪��P4�����ף�s��+5O2��g���TP4O10��s����H=-2983.2kJ/mol
P�����ף�s��+$\frac{5}{4}$O2��g���T$\frac{1}{4}$P4O10��s����H=-738.5kJ/mol
��д������ת��Ϊ�����Ȼ�ѧ����ʽP4�����ף�s��=4P�����ף�s����H=-29.2kJ/mol��