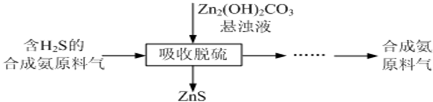
2.下列实验装置能达到实验目的是( )
| A. |  进行喷泉实验 | B. | 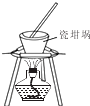 加热熔融(NaOH) | ||
| C. |  验证镁片与稀盐酸反应放热 | D. | 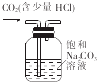 除去CO2中的少量HCl |
19.下列溶液中,溶质的物质的量浓度为1mol•L-1 的是( )
0 173684 173692 173698 173702 173708 173710 173714 173720 173722 173728 173734 173738 173740 173744 173750 173752 173758 173762 173764 173768 173770 173774 173776 173778 173779 173780 173782 173783 173784 173786 173788 173792 173794 173798 173800 173804 173810 173812 173818 173822 173824 173828 173834 173840 173842 173848 173852 173854 173860 173864 173870 173878 203614
| A. | 将80 g NaOH溶于2 L 水所得的溶液 | |
| B. | 将0.5 mol•L-1的NaNO3溶液100 mL 加热蒸发掉50 g水所得的溶液 | |
| C. | 将40 g NaOH 溶于水并配成1 L的溶液 | |
| D. | 含K+为4 mol•L-1的K2SO4溶液 |





 ;
; .
. 是一种重要的药物合成中间体,请结合题目所给信息,
是一种重要的药物合成中间体,请结合题目所给信息, 为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.