3.N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是 .
.
(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)?4NO2(g)+O2(g);△H>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将不变(填“增大”、“减小”、“不变”).
②如表为反应在T1温度下的部分实验数据:
则500s内N2O5的分解速率为0.00296 mol•L-1•s-1.
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol•L-1,则T2<T1(填>、<或=).
(3)现以H2、O2、熔融Na2CO3组成的燃料电池采用电解法制备N2O5,装置如图所示,其中Y为CO2.
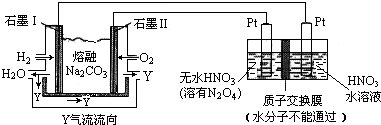
写出石墨Ⅰ电极上发生反应的电极反应式H2+CO32--2e-═H2O+CO2,N2O5在电解池的阳极区生成(填“阳极”或“阴极”).
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是
 .
.(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)?4NO2(g)+O2(g);△H>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将不变(填“增大”、“减小”、“不变”).
②如表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol•L-1,则T2<T1(填>、<或=).
(3)现以H2、O2、熔融Na2CO3组成的燃料电池采用电解法制备N2O5,装置如图所示,其中Y为CO2.

写出石墨Ⅰ电极上发生反应的电极反应式H2+CO32--2e-═H2O+CO2,N2O5在电解池的阳极区生成(填“阳极”或“阴极”).
12.下列有关电解质溶液说法正确的是( )
| A. | pH均为3的溶液,加水稀释10倍后的pH:HCl>H2SO4>CH3COOH | |
| B. | 浓度均为0.1mol•L-1的氨水和氯化铵溶液,水电离出的c(H+)前者小于后者 | |
| C. | 碳酸钠溶液中存在:c(OH-)=c(H+)+c(H2CO3)+c(CO32-) | |
| D. | 0.1mol/L Na2CO3溶液35℃时的碱性比25℃时强,说明盐类水解反应是放热反应 |
10.已知4A+5B→4C+2D,则关于反应速率,正确的关系是( )
0 173430 173438 173444 173448 173454 173456 173460 173466 173468 173474 173480 173484 173486 173490 173496 173498 173504 173508 173510 173514 173516 173520 173522 173524 173525 173526 173528 173529 173530 173532 173534 173538 173540 173544 173546 173550 173556 173558 173564 173568 173570 173574 173580 173586 173588 173594 173598 173600 173606 173610 173616 173624 203614
| A. | 4V(A)=5V(B) | B. | 5V(B)=6VD | C. | 2V(A)=3VD | D. | 4V(B)=5VC |
 在固定容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g)随温度升高,混合气体的颜色变深.回答下列问题:
在固定容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g)随温度升高,混合气体的颜色变深.回答下列问题: