3.下列离子方程式正确的是( )
| A. | NaClO溶液中通入少量SO2:ClO-+SO2+H2O=2H++SO42-+Cl- | |
| B. | FeCl3溶液中通入过量H2S气体:2Fe3++3H2S=2FeS↓+S↓+6H+ | |
| C. | Na2CO3溶液中通入少量Cl2:2CO32-+Cl2+H2O=ClO-+Cl-+2HCO3- | |
| D. | NaHSO3溶液中通入少量Cl2:HSO3-+Cl2+H2O=3H++SO42-+2Cl- |
20.蓄电池放电时是起原电池的作用,在充电时起电解池的作用.下式是爱迪生蓄电池分别在充电、放电时的反应:Fe+NiO2+2H2O$?_{充电}^{放电}$Fe(OH)2+Ni(OH)2下列各种推断中正确的是( )
| A. | 充电时铁做负极,NiO2做正极 | |
| B. | 放电时阴极上的电极反应为:Fe(OH)2+2e-=Fe+2OH- | |
| C. | 放电时,电解质溶液中的阴离子是向正极方向移动 | |
| D. | 蓄电池的两个电极必须浸入在碱性溶液中 |
19.下列关于二氧化硅的说法正确的是( )
| A. | 二氧化硅是酸性氧化物,因此能与水反应生成硅酸 | |
| B. | 用二氧化硅制取单质硅时,当生成2.24 L气体(标准状况)时,得到2.8 g硅 | |
| C. | 二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆 | |
| D. | 二氧化硅不能与碳酸钠溶液反应,但能与碳酸钠固体在高温时发生反应 |
18.已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡,下列说法正确的是( )
 ?
?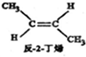 ,△H=-4.2kJ.mol-1
,△H=-4.2kJ.mol-1
 (g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.
(g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.
 ?
? ,△H=-4.2kJ.mol-1
,△H=-4.2kJ.mol-1 (g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.
(g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.| A. | 反-2-丁烯比顺-2-丁烯稳定 | |
| B. | 顺-2-丁烯的燃烧热数值比反-2-丁烯小 | |
| C. | 减压和升温有利于平衡向生成正丁烷反应方向移动 | |
| D. | 反-2-丁烯氢化的热化学方程式为: (g)+H2(g)?CH3CH2CH2CH3(g),△H=-123.1kJ•mol-1 (g)+H2(g)?CH3CH2CH2CH3(g),△H=-123.1kJ•mol-1 |
17.体积为1L的某溶液中可能含有Cl-、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$、CO${\;}_{3}^{2-}$、NH${\;}_{4}^{+}$、Fe3+、Al2+、Ba2+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生的白色沉淀迅速变为灰绿色;过滤、洗涤、灼烧,得到1.6g固体;向上述滤液中加入足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.下列叙述正确的是( )
| A. | 溶液中的主要离子仅为SO${\;}_{3}^{2-}$、Fe2+、NH${\;}_{4}^{+}$ | |
| B. | Cl-一定存在,且c(Cl-)=0.2 mol.L-l | |
| C. | 向原溶液中加入硫酸,可能有气体生成 | |
| D. | CO${\;}_{3}^{2-}$、Al2+一定不存在,K+可能存在 |
16.在标准状况下,如果0.5L氧气含有m个氧气分子,则阿伏加德罗常数可表示为( )
0 173360 173368 173374 173378 173384 173386 173390 173396 173398 173404 173410 173414 173416 173420 173426 173428 173434 173438 173440 173444 173446 173450 173452 173454 173455 173456 173458 173459 173460 173462 173464 173468 173470 173474 173476 173480 173486 173488 173494 173498 173500 173504 173510 173516 173518 173524 173528 173530 173536 173540 173546 173554 203614
| A. | m/22.4 | B. | 44.8m | C. | 22.4m | D. | m/32 |
 进入秋冬季节后,郑州市频现雾霾天气,给人们的出行带来极大的不便和危害,人们“谈霾色变”.目前郑州市汽车保有量达230万量,汽车尾气的污染是引起雾霾的主要因素之一,NO和CO是汽车尾气的主要污染物.
进入秋冬季节后,郑州市频现雾霾天气,给人们的出行带来极大的不便和危害,人们“谈霾色变”.目前郑州市汽车保有量达230万量,汽车尾气的污染是引起雾霾的主要因素之一,NO和CO是汽车尾气的主要污染物.