8.(1)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,该反应的热化学方程式为B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=-2165kJ/mol.又已知:H2O(g)=H2O(l);△H2=-44.0kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是1016.5kJ.
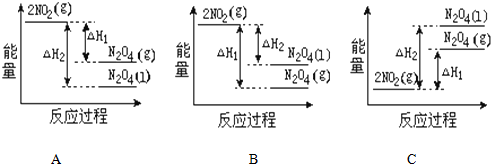
(2)已知:2NO2(g)═N2O4(g)△H1 2NO2(g)═N2O4(l)△H2
下列能量变化示意图中,正确的是(选填字母)A.
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(s,石墨)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2 599kJ•mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变(列出简单的计算式):+226.7kJ•mol-1.
(4)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇气体(结构简式为CH3OH). 已知某些化学键的键能数据如表:
已知CO中的C与O之间为叁键连接,则工业制备甲醇的热化学方程式为CO(g)+2H2(g)?CH3OH (g)△H=-116 kJ•mol-1.
(2)已知:2NO2(g)═N2O4(g)△H1 2NO2(g)═N2O4(l)△H2
下列能量变化示意图中,正确的是(选填字母)A.

(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(s,石墨)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2 599kJ•mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变(列出简单的计算式):+226.7kJ•mol-1.
(4)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇气体(结构简式为CH3OH). 已知某些化学键的键能数据如表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
7.到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.

(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O (l)△H=-704KJ/mol
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关.
①如图1是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请计算每生成1mol NH3放出热量为:46KJ
②若已知下列数据:
试根据表中及图中数据计算N-H的键能390kJ•mol-1
③若起始时向容器内放入1mol N2和3mol H2,达平衡后N2的转化率为20%,则反应放出的热量为18.4kJ
④如图2表示在密闭容器中反应:N2(g)+3H2(g)?2NH3(g)△H<0,达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是升高温度;若增大压强时,反应速度变化情况画在c~d处.
(3)①二氧化碳的捕集、利用是我国能源领域的一个重要战略方向.工业上用CO2和H2反应合成二甲醚.已知:
CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H1=-53.7kJ.mol-1
CH3OH3(g)+H2O(g)═2CH3OH(g)△H2=+23.47kJ.mol-1
则2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)△H3=-130.8kJ.mol-1
②一定条件下,上述合成二甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是b(填代号).
a.逆反应速率先增大后减小 b.H2的转化率增大
c.CO2的体积百分含量减小 d.容器中二甲醚的浓度增大
③在一定条件下,将CO2和H2以体积比1:2置于密闭容器中发生上述反应:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)
下列能说明反应达到平衡状态的是abd
a.体系压强不变 b.CO2和H2的体积比不变
c.混合气体的密度不变 d.混合气体的平均相对分子质量不变.

(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O (l)△H=-704KJ/mol
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关.
①如图1是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请计算每生成1mol NH3放出热量为:46KJ
②若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ•mol-1 | 435 | 943 |
③若起始时向容器内放入1mol N2和3mol H2,达平衡后N2的转化率为20%,则反应放出的热量为18.4kJ
④如图2表示在密闭容器中反应:N2(g)+3H2(g)?2NH3(g)△H<0,达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是升高温度;若增大压强时,反应速度变化情况画在c~d处.
(3)①二氧化碳的捕集、利用是我国能源领域的一个重要战略方向.工业上用CO2和H2反应合成二甲醚.已知:
CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H1=-53.7kJ.mol-1
CH3OH3(g)+H2O(g)═2CH3OH(g)△H2=+23.47kJ.mol-1
则2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)△H3=-130.8kJ.mol-1
②一定条件下,上述合成二甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是b(填代号).
a.逆反应速率先增大后减小 b.H2的转化率增大
c.CO2的体积百分含量减小 d.容器中二甲醚的浓度增大
③在一定条件下,将CO2和H2以体积比1:2置于密闭容器中发生上述反应:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)
下列能说明反应达到平衡状态的是abd
a.体系压强不变 b.CO2和H2的体积比不变
c.混合气体的密度不变 d.混合气体的平均相对分子质量不变.
6.下列有关热化学方程式的叙述正确的是( )
| A. | 已知S(单斜,s)=S(正交,s)△H<0,则单斜硫比正交硫稳定 | |
| B. | HCl和NaOH反应的中加热△H=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| C. | 已知S(g)+O2(g)═SO2(g)△H1<0;S(s)+O2(g)═SO2(g)△H2<0 则△H1<△H2 | |
| D. | 下列反应中,反应物的总能量E1与生成物的总能量E2一定相等$\stackrel{A+B}{反应物总能量{E}_{1}}$$\stackrel{发生反应A+B=C+D}{→}$$\stackrel{C+D}{生成物总能量{E}_{2}}$ |
5.已知热化学方程式:SO2(g)+$\frac{1}{2}$O2(g)=SO3(g)△H=-98.32kJ/mol,下列表述正确的是( )
0 173226 173234 173240 173244 173250 173252 173256 173262 173264 173270 173276 173280 173282 173286 173292 173294 173300 173304 173306 173310 173312 173316 173318 173320 173321 173322 173324 173325 173326 173328 173330 173334 173336 173340 173342 173346 173352 173354 173360 173364 173366 173370 173376 173382 173384 173390 173394 173396 173402 173406 173412 173420 203614
| A. | 在容器中充入2mol SO2和1mol O2充分反应,最终放出的热量等于196.64kJ | |
| B. | 在容器中当有2mol SO2和1mol O2发生反应时,放出的热量等于196.64kJ | |
| C. | 在容器中当有4mol SO2和2mol O2发生反应时,反应SO2(g)+$\frac{1}{2}$O2(g)=SO3(g)的反应热为-393.28kJ/mol | |
| D. | 在容器中当有4mol SO2和2mol O2发生反应时,反应SO2(g)+$\frac{1}{2}$O2(g)=SO3(g)的反应热为98.32kJ/mol |
 甲醇是一种重要的化工原料.有着重要的用途和应用前景.
甲醇是一种重要的化工原料.有着重要的用途和应用前景.