14.在25℃、1.01×105Pa下,将22g CO2通入到750mL 1.0mol•L-1的NaOH溶液中充分反应,放出x kJ热量.在该条件下1molCO2通入到2L 1.0mol•L-1的NaOH溶液中充分反应,放出ykJ热量,则CO2与NaOH反应生成NaHCO3的热化学反应方程式为( )
| A. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2y-x) kJ•mol-1 | |
| B. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(4x-y) kJ•mol-1 | |
| C. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y) kJ•mol-1 | |
| D. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(8x-2y) kJ•mol-1 |
13.某同学设计如图元素周期表,已知Z元素的最外层电子数是次外层的3倍.空格中均有对应的元素填充.以下说法正确的是( )


| A. | 白格中都是主族元素,灰格中都是副族元素 | |
| B. | X和Z形成的化合物只有两种 | |
| C. | X、Y元素最高价氧化物对应的水化物酸性:X>Y | |
| D. | X、Y、Z的气态氢化物中最稳定的是:X的氢化物 |
9.元素的原子结构决定其性质和在周期表中的位置.下列说法正确的是( )
| A. | P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强 | |
| B. | 多电子原子中,在离核较近的区域内运动的电子能量较高 | |
| C. | 元素原子的最外层电子数等于元素的最高化合价 | |
| D. | 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
5. A、B、C三种短周期元素在周期表中的相对位置如图所示,已知A、C分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则以下说法判断正确的是( )
A、B、C三种短周期元素在周期表中的相对位置如图所示,已知A、C分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则以下说法判断正确的是( )
0 173087 173095 173101 173105 173111 173113 173117 173123 173125 173131 173137 173141 173143 173147 173153 173155 173161 173165 173167 173171 173173 173177 173179 173181 173182 173183 173185 173186 173187 173189 173191 173195 173197 173201 173203 173207 173213 173215 173221 173225 173227 173231 173237 173243 173245 173251 173255 173257 173263 173267 173273 173281 203614
 A、B、C三种短周期元素在周期表中的相对位置如图所示,已知A、C分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则以下说法判断正确的是( )
A、B、C三种短周期元素在周期表中的相对位置如图所示,已知A、C分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则以下说法判断正确的是( )| A. | B与C均不存在同素异形体 | B. | X一定是酸性氧化物 | ||
| C. | B的氢化物比A、C的氢化物稳定 | D. | A与B形成的化合物X有3种 |
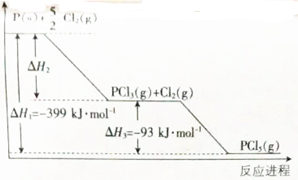
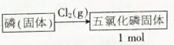

 A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等. ,C的氢化物与B的氢化物的稳定性强弱顺序为HF>H2S(填化学式).
,C的氢化物与B的氢化物的稳定性强弱顺序为HF>H2S(填化学式).
 ;写出它与原子半径最小的原子形成10电子且为正四面体结构的化合物的电子式
;写出它与原子半径最小的原子形成10电子且为正四面体结构的化合物的电子式 ,用电子式表示⑤和⑧形成化合物的过程
,用电子式表示⑤和⑧形成化合物的过程 .
. 有A、B、C、D、E五种短周期元素,其中A、B、C三元素在周期表中位置如下表所示.该三元素的原子序数之和为41.A和D的单质在不同条件下可以反应生成D2A(白色固体)和D2A2(淡黄色固体)两种化合物.E单质在C单质中燃烧时产生苍白色火焰,生成物的水溶液能使石蕊试液变红.
有A、B、C、D、E五种短周期元素,其中A、B、C三元素在周期表中位置如下表所示.该三元素的原子序数之和为41.A和D的单质在不同条件下可以反应生成D2A(白色固体)和D2A2(淡黄色固体)两种化合物.E单质在C单质中燃烧时产生苍白色火焰,生成物的水溶液能使石蕊试液变红.