3.表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素的符号:①N,⑥Si,⑦S.
(2)在这些元素中,最活泼的金属元素是K (填元素符号,下同),最活泼的非金属元素是F,最不活泼的元素是Ar.
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4填化学式,下同),碱性最强的是KOH,两性的氢氧化物是Al(OH)3,写出这三者之间相互反应的化学方程式:HClO4+KOH=KClO4+H2O,3HClO4+Al(OH)3=Al(ClO4)3+3H2O,KOH+Al(OH)3=KAlO2+2H2O.
(4)在这些元素中,原子半径最小的是F (填化学式,下同),原子半径最大的是K.③与⑧的简单离子的半径大小为Cl->Na+.
(5)在③与④中,化学性质较活泼的是钠(填化学名称)
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | (11) | (12) |
(2)在这些元素中,最活泼的金属元素是K (填元素符号,下同),最活泼的非金属元素是F,最不活泼的元素是Ar.
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4填化学式,下同),碱性最强的是KOH,两性的氢氧化物是Al(OH)3,写出这三者之间相互反应的化学方程式:HClO4+KOH=KClO4+H2O,3HClO4+Al(OH)3=Al(ClO4)3+3H2O,KOH+Al(OH)3=KAlO2+2H2O.
(4)在这些元素中,原子半径最小的是F (填化学式,下同),原子半径最大的是K.③与⑧的简单离子的半径大小为Cl->Na+.
(5)在③与④中,化学性质较活泼的是钠(填化学名称)
2.如表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①N,⑥Si,⑦S.
(2)画出原子的结构示意图:④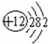 ,⑧
,⑧ ;
;
(3)在表中有编号的元素中,金属性最强的元素是K,非金属性最强的元素是F,用电子式表示它们形成化合物的过程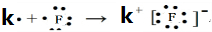 .最不活泼的元素是Ar.(以上均填元素名称)
.最不活泼的元素是Ar.(以上均填元素名称)
(4)元素③、⑩、的氢氧化物碱性由强到弱的顺序KOH>NaOH;元素⑥、⑦、⑧的氢化物稳定性由弱到强的顺序SiH4<H2S<HCl(均用化学式填空)
(5)周期中有一种元素,其最高价氧化物的水化物与同周期其它元素最高价氧化物的水化物所属物质类型都不同,用离子方程式表示该水化物分别与烧碱溶液和稀硫酸的反应:Al(OH)3+OH-=AlO2-+2H2O、Al(OH)3+3H+=Al3++3H2O;.
(6)与①和⑥都相邻的一种元素A,它有多种不同形态的单质,其中一种常用作原电池的电极,它与⑦的最高价氧化物的水化物浓溶液在加热时能反应,写出化学反应方程式:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O
(7)写出能验证⑦的非金属性强于A的化学反应的离子方程式:CO32-+2H+=CO2↑+H2O.
 | ⅠA | ⅡA | ⅢA | ⅠVA | VA | VⅠA | VⅡA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(2)画出原子的结构示意图:④
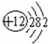 ,⑧
,⑧ ;
;(3)在表中有编号的元素中,金属性最强的元素是K,非金属性最强的元素是F,用电子式表示它们形成化合物的过程
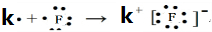 .最不活泼的元素是Ar.(以上均填元素名称)
.最不活泼的元素是Ar.(以上均填元素名称)(4)元素③、⑩、的氢氧化物碱性由强到弱的顺序KOH>NaOH;元素⑥、⑦、⑧的氢化物稳定性由弱到强的顺序SiH4<H2S<HCl(均用化学式填空)
(5)周期中有一种元素,其最高价氧化物的水化物与同周期其它元素最高价氧化物的水化物所属物质类型都不同,用离子方程式表示该水化物分别与烧碱溶液和稀硫酸的反应:Al(OH)3+OH-=AlO2-+2H2O、Al(OH)3+3H+=Al3++3H2O;.
(6)与①和⑥都相邻的一种元素A,它有多种不同形态的单质,其中一种常用作原电池的电极,它与⑦的最高价氧化物的水化物浓溶液在加热时能反应,写出化学反应方程式:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O
(7)写出能验证⑦的非金属性强于A的化学反应的离子方程式:CO32-+2H+=CO2↑+H2O.
2.给铁制器皿上镀铜,应该使用的电镀液是( )
| A. | FeCl3 | B. | CuSO4 | C. | FeSO4 | D. | NaCl |
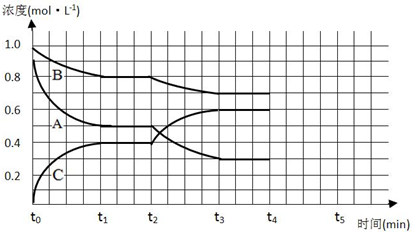
1.在一固定体积的1L的密闭容器中,加入2molA和1molB发生如下反应:2A(g)+B(g)?3C(g)+D(s),达到平衡时C的浓度为1.2mol/L.若维持容器体积和温度不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2mol/L的是( )
| A. | 4molA+2molB | |
| B. | 3molC+1molD+1molB | |
| C. | 3molC+0.8molD | |
| D. | 1.6molA+0.8molB+0.6molC+0.3molD |
20.下列有关设计的方案能达到实验目的是( )
| A. | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液,有气体生成,溶液未呈血红色,说明稀硝酸不能将Fe氧化为Fe3+ | |
| B. | 除去FeCl3溶液中少量Cu2+:向含有少量Cu2+的FeCl3溶液中加入适量铁粉,充分反应后过滤 | |
| C. | 比较Fe(OH)3和Al(OH)3的Ksp:向0.1mol•L-1的FeCl3溶液中滴加0.1mol•L-1氨水至不再产生沉淀,然后再滴入0.1mol•L-1A1Cl3溶液,观察现象 | |
| D. | 验证氧化性Fe3+<Br2<Cl2;向试管中依次加入1mL0.1mol•L-1FeBr2溶液、几滴KSCN溶液和1mL苯,然后逐滴加入氯水,并缓缓振荡,直到氯水过量,观察整个过程中有机层和水层中的现象. |
19.2mol•L-1的盐酸和硫酸各100mL,分别加入等质量的铁粉,反应后生成的气体质量比为2:3,则往盐酸中加入铁粉的物质的量为( )
| A. | 0.05mol | B. | 0.075mol | C. | 0.15mol | D. | 0.2mol |
17.溴化碘(IBr)是一种卤素互化物,它的化学性质活泼,能与大多数金属反应,也能与某些分金属单质反应,并能与水发生如下反应:IBr+H2O→HBr+HIO,下列有关溴化碘的叙述不正确的是( )
0 173086 173094 173100 173104 173110 173112 173116 173122 173124 173130 173136 173140 173142 173146 173152 173154 173160 173164 173166 173170 173172 173176 173178 173180 173181 173182 173184 173185 173186 173188 173190 173194 173196 173200 173202 173206 173212 173214 173220 173224 173226 173230 173236 173242 173244 173250 173254 173256 173262 173266 173272 173280 203614
| A. | 溴化碘与Br2、I2具有相似的化学性质 | |
| B. | 在许多反应中,IBr是一种强氧化剂 | |
| C. | 在溴化碘与水反应中,IBr既是氧化剂,又是还原剂 | |
| D. | 溴化碘与氢氧化钠溶液反应时可生成两种盐 |

 .
. .
.