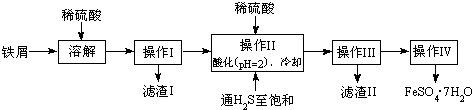
18.绿矾(FeSO4•7H2O)是治疗缺铁性贫血药品的重要成分.如图是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
查询资料,得有关物质的数据如表:
(1)写出Fe和Fe2O3在硫酸溶液中发生反应的离子方程式为Fe+2H+=Fe2++H2↑、Fe2O3+6H+=2Fe3++3H2O、2Fe3++Fe=3Fe2+;.
(2)操作II中,通入硫化氢至饱和的目的是:①除去溶液中的Sn2+离子;②防止Fe2+被氧化;③在溶液中用硫酸酸化至pH=2的目的是防止Fe2+离子生成沉淀.
(3)操作IV的顺序依次为蒸发浓缩、冷却结晶、过滤洗涤.
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;②降低洗涤过程中FeSO4•7H2O的损耗.
(5)已知常温下,Ksp[Fe(OH)2]=1.64×10-14,则求得反应:Fe2++2H2O?Fe(OH)2+2H+的平衡常数为:0.6×10-14(保留1位小数)
(6)测定绿矾产品中Fe2+含量的方法是:a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.计算上述样品中FeSO4•7H2O的质量分数为97.5%.(保留3位小数)

查询资料,得有关物质的数据如表:
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(2)操作II中,通入硫化氢至饱和的目的是:①除去溶液中的Sn2+离子;②防止Fe2+被氧化;③在溶液中用硫酸酸化至pH=2的目的是防止Fe2+离子生成沉淀.
(3)操作IV的顺序依次为蒸发浓缩、冷却结晶、过滤洗涤.
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;②降低洗涤过程中FeSO4•7H2O的损耗.
(5)已知常温下,Ksp[Fe(OH)2]=1.64×10-14,则求得反应:Fe2++2H2O?Fe(OH)2+2H+的平衡常数为:0.6×10-14(保留1位小数)
(6)测定绿矾产品中Fe2+含量的方法是:a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.计算上述样品中FeSO4•7H2O的质量分数为97.5%.(保留3位小数)
14. 在2L恒容密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L恒容密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:
(1)写出该反应的平衡常数表达式:$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)×c({O}_{2})}$,已知K(300℃)>K(350℃),则该反应正反应为放热 反应(填“放热”或“吸热”),升高温度,正反应速率增大,(填“增大”“减小”或“不变”)
(2)图中表示NO2的变化的曲线是b,用氧气表示0-2s内该反应平均反应速率v(O2)=1.5×10-3mol•L-1•s-1.
(3)求达平衡时NO的转化率为65%.
(4)能说明该反应已经达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v(NO)逆=2v(O2)正 d.容器内的密度保持不变
(5)能够使该反应的反应速率增大,且平衡向正反应方向移动的是b.
a.及时分离出NO2气体 b.增大O2的浓度.c.适当升高温度 d.使用高效催化剂.
 在2L恒容密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L恒容密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2的变化的曲线是b,用氧气表示0-2s内该反应平均反应速率v(O2)=1.5×10-3mol•L-1•s-1.
(3)求达平衡时NO的转化率为65%.
(4)能说明该反应已经达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v(NO)逆=2v(O2)正 d.容器内的密度保持不变
(5)能够使该反应的反应速率增大,且平衡向正反应方向移动的是b.
a.及时分离出NO2气体 b.增大O2的浓度.c.适当升高温度 d.使用高效催化剂.
11. 在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
(1)上述反应是(填“是”或“不是”)可逆反应,在第5s时,NO的转化率为65%.
(2)如图中表示NO2变化曲线的是b.用O2表示0~2s内该反应的平均速率v=1.5×10-3mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)、铅蓄电池是常用的化学电源,其电极材料是Pb和PbO2,电解液为稀硫酸.工作时该电池总反应式为:PbO2+Pb+2H2SO4═2PbSO4+2H2O,据此判断:
①工作时正极反应为PbO2+4H++SO42-+2e-═PbSO4+2H2O.
②工作时,电解质溶液的pH值增大(“增大”、“减小”或“不变”)
③工作时,电解质溶液中阴离子移向负极.
(5)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知0.4mol液态肼与足量液态双氧水反应,生成水蒸气和氮气,放出256.652kJ的热量.
①反应的热化学方程式为N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63 kJ•mol-1.
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是产物不会造成环境污染.
③发射卫星可用肼为燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气.已知:
N2(g)+2O2(g)═2NO2(g),△H=+67.7kJ•mol-1
N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-534kJ•mol-1
肼和二氧化氮反应的热化学方程式为N2H4(g)+NO2(g)═$\frac{3}{2}$N2(g)+2H2O(g)△H=-567.85 kJ•mol-1.
 在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示NO2变化曲线的是b.用O2表示0~2s内该反应的平均速率v=1.5×10-3mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)、铅蓄电池是常用的化学电源,其电极材料是Pb和PbO2,电解液为稀硫酸.工作时该电池总反应式为:PbO2+Pb+2H2SO4═2PbSO4+2H2O,据此判断:
①工作时正极反应为PbO2+4H++SO42-+2e-═PbSO4+2H2O.
②工作时,电解质溶液的pH值增大(“增大”、“减小”或“不变”)
③工作时,电解质溶液中阴离子移向负极.
(5)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知0.4mol液态肼与足量液态双氧水反应,生成水蒸气和氮气,放出256.652kJ的热量.
①反应的热化学方程式为N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63 kJ•mol-1.
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是产物不会造成环境污染.
③发射卫星可用肼为燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气.已知:
N2(g)+2O2(g)═2NO2(g),△H=+67.7kJ•mol-1
N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-534kJ•mol-1
肼和二氧化氮反应的热化学方程式为N2H4(g)+NO2(g)═$\frac{3}{2}$N2(g)+2H2O(g)△H=-567.85 kJ•mol-1.
10.400℃时,往一密闭容器中通入 4molSO2和 2molO2,反应达到平衡时,容器内压强是反应前的四分之三.此时 SO2的转化率为( )
0 172552 172560 172566 172570 172576 172578 172582 172588 172590 172596 172602 172606 172608 172612 172618 172620 172626 172630 172632 172636 172638 172642 172644 172646 172647 172648 172650 172651 172652 172654 172656 172660 172662 172666 172668 172672 172678 172680 172686 172690 172692 172696 172702 172708 172710 172716 172720 172722 172728 172732 172738 172746 203614
| A. | 75% | B. | 25% | C. | 37.5% | D. | 81% |



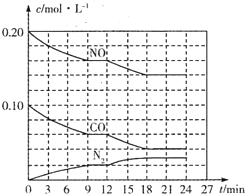 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质.