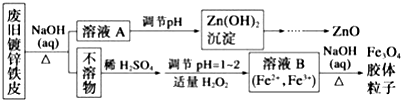
2.用 FeCl3酸性溶液脱除 H2S后的废液,通过控制电压电解得以再生.某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/LFeCl2溶液,研究废液再生机理.记录如下(a、b、c代表电压值:)
(1)用 FeCl3酸性溶液脱除 H2S的离子方程式为2Fe3++H2S=2Fe2++2H++S↓.
(2)I中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化.写出有关反应的方程式和电极反应式2Cl--2e-=Cl2↑,Cl2+2Fe2+=2Fe3++2Cl-.
(3)由II 推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有还原性.电极反应式为Fe2+-e-=Fe3+.
(4)II中虽未检测出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如下:
①NaCl溶液的浓度是0.2mol/L.
②与II对比,可得出的结论:ABC
A.通过控制电压,验证了Fe2+先于Cl-放电
B.电压过小,Cl- 可能不放电
C.通过控制电压,证实了产生Fe3+的两种原因都成立
D.通过控制电压,证实了产生Fe3+一定仅是由于生成的Cl2将Fe2+氧化.
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(2)I中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化.写出有关反应的方程式和电极反应式2Cl--2e-=Cl2↑,Cl2+2Fe2+=2Fe3++2Cl-.
(3)由II 推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有还原性.电极反应式为Fe2+-e-=Fe3+.
(4)II中虽未检测出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
②与II对比,可得出的结论:ABC
A.通过控制电压,验证了Fe2+先于Cl-放电
B.电压过小,Cl- 可能不放电
C.通过控制电压,证实了产生Fe3+的两种原因都成立
D.通过控制电压,证实了产生Fe3+一定仅是由于生成的Cl2将Fe2+氧化.
1.向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色.如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色(I2被氧化为 HIO3).下列说法正确的是( )
| A. | 整个过程中的还原剂只有I2 | |
| B. | CCl4层由紫色变成无色的化学反应方程式为:I2+5Cl2+6H2O=2HIO3+10HCl | |
| C. | 若用KI和Cl2反应制1molKIO3,至少需要56LCl2(标准状况) | |
| D. | 把 KI换成NBr,则CCl4层变为红棕色.继续滴加氯水,CCl4层的颜色没有变化,则Cl2、HIO3、HBrO3氧化性由弱到强的顺序是:HBrO3<Cl2<HIO3 |
20.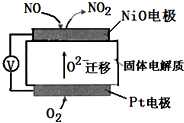 通过 NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法正确的是( )
通过 NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法正确的是( )
 通过 NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法正确的是( )
通过 NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法正确的是( )| A. | Pt 电极上发生的是氧化反应 | |
| B. | O2-向正极迁移 | |
| C. | 负极的电极反应式为:NO-2e-+O2-=NO2 | |
| D. | 正极的电极反应式为:O2+2H2O+4e-=4OH- |
19.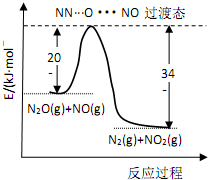 由 N2O和NO反应生成N2和NO2的能量变化如图所示,下列说法正确的是( )
由 N2O和NO反应生成N2和NO2的能量变化如图所示,下列说法正确的是( )
 由 N2O和NO反应生成N2和NO2的能量变化如图所示,下列说法正确的是( )
由 N2O和NO反应生成N2和NO2的能量变化如图所示,下列说法正确的是( )| A. | 由图分析 N2O(g) 的能量一定高于 NO2(g)+N2(g) | |
| B. | 反应过程中没有发生化学键的断裂和化学键的生成 | |
| C. | 若生成 1mol N2(g),其△H=-139kJ•mol-1 | |
| D. | 由图可知 N2+NO2=N2O+NO△H=+139kJ•mol-1, 若使用催化剂还可以减小反应的热效应 |
18.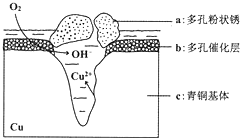 如图所示为青铜器在潮湿环境中发生的电化学腐蚀的示意图,下列说法错误的是( )
如图所示为青铜器在潮湿环境中发生的电化学腐蚀的示意图,下列说法错误的是( )
 如图所示为青铜器在潮湿环境中发生的电化学腐蚀的示意图,下列说法错误的是( )
如图所示为青铜器在潮湿环境中发生的电化学腐蚀的示意图,下列说法错误的是( )| A. | 腐蚀过程中,铜被氧化 | |
| B. | 已知环境中的 Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈Cu2(OH)3Cl,则其离子方程式为:2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓ | |
| C. | 若生成 4.29 g Cu2(OH)3Cl,则理论上耗氧体积定为 0.448 L | |
| D. | 正极的电极反应式为:O2+4e-+2H2O=4OH- |
17.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 粗铜板作阳极,电解硫酸铜溶液 | 粗铜溶解,纯铜在阴极上析出 | Cu 放电是氧化剂 |
| B | 向银氨溶液中滴加几滴乙醛后 水浴加热 | 银附着在试管壁上 | 乙醛发生还原反 应 |
| C | 向含 I-的无色溶液中滴加少量 新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 氧化性:Cl2>I2 |
| D | 向 FeSO4溶液中先滴入 KSCN 溶液再滴加 H2O2 溶液 | 加入 H2O2后溶液变成血红色 | Fe2+既有氧化性又 有还原性 |
| A. | A | B. | B | C. | C | D. | D |
16.下列有关物质分类的描述正确的是( )
| A. | 金属氧化物一定是碱性氧化物 | |
| B. | SO2水溶液能导电,所以 SO2是电解质 | |
| C. | 胶体是纯净物,可以用丁达尔效应鉴别胶体和溶液 | |
| D. | 人们在认识事物时往往需要采用多种分类方法,来弥补单一分类方法的不足 |
15.下列装置中发生的化学反应不属于氧化还原反应的是( )
| A. | 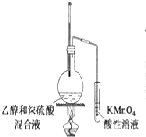 | B. |  | C. | 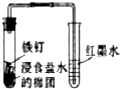 | D. |  |
14.NA为阿伏伽德罗常数的值,下列说法正确的是( )
0 172333 172341 172347 172351 172357 172359 172363 172369 172371 172377 172383 172387 172389 172393 172399 172401 172407 172411 172413 172417 172419 172423 172425 172427 172428 172429 172431 172432 172433 172435 172437 172441 172443 172447 172449 172453 172459 172461 172467 172471 172473 172477 172483 172489 172491 172497 172501 172503 172509 172513 172519 172527 203614
| A. | 标准状况下,22.4 L N2和 H2 混合气中含 NA个原子 | |
| B. | 3 mol 单质 Fe 完全转变为 Fe3O4,失去 8NA个电子 | |
| C. | 2 L 0.5 mol•L-1硫酸钾溶液中,含有 NA个阳离子 | |
| D. | 标准状况下,2128 mL 甲醛含有 2.85NA个电子 |