17.可逆反应:3A(气)?3B(?)+C(?);△H>0,随着温度升高,气体平均相对分子质量变小,则下列判断正确的是( )
| A. | B和C可能都是固体 | B. | B和C一定都是气体 | ||
| C. | 若C为固体,则B一定是气体 | D. | B和C可能都是液体酶 |
16.下列说法正确的是( )
(1)增加水的量或升高温度,一定可以加快镁跟水的反应速率
(2)增大硫酸的浓度,一定可以加快锌与硫酸反应制取氢气的速率
(3)对于反应CaCO3(s)?CaO(s)+CO2(g),增加CaCO3的量,可以加快正反应速率,而增加CaO或CO2的浓度,则可以加快逆反应速率
(4)对于反应3H2(g)+N2(g)?2NH3(g),在密闭容器中进行(固定体积),现充入氦气,由于容器中压强增大,则化学反应速率加快
(5)对于反应3H2(g)+N2(g)?2NH3(g),使用适合催化剂,正逆反应速率同等程度加快.
(1)增加水的量或升高温度,一定可以加快镁跟水的反应速率
(2)增大硫酸的浓度,一定可以加快锌与硫酸反应制取氢气的速率
(3)对于反应CaCO3(s)?CaO(s)+CO2(g),增加CaCO3的量,可以加快正反应速率,而增加CaO或CO2的浓度,则可以加快逆反应速率
(4)对于反应3H2(g)+N2(g)?2NH3(g),在密闭容器中进行(固定体积),现充入氦气,由于容器中压强增大,则化学反应速率加快
(5)对于反应3H2(g)+N2(g)?2NH3(g),使用适合催化剂,正逆反应速率同等程度加快.
| A. | (1)(2) | B. | (1)(2)(3) | C. | (1)(2)(3)(4) | D. | (5) |
15.在同温同压下,下列各组热化学方程式中△H2>△H1的是( )
| A. | 2H2(g)+O2(g)═2H2O(g),△H1; 2H2(g)+O2(g)═2H2O(l),△H2 | |
| B. | S(s)+O2(g)═SO2(g),△H1; S(g)+O2(g)═SO2(g),△H2 | |
| C. | C(s)+$\frac{1}{2}$ O2(g)═CO(g),△H1; C(s)+O2(g)═CO2(g),△H2 | |
| D. | H2(g)+Cl2(g)═2HCl(g),△H1; $\frac{1}{2}$H2(g)+$\frac{1}{2}$ Cl2(g)═HCl(g),△H2 |
14.下列图象表达正确的是( )
| A. | 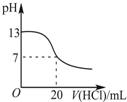 表示25℃时,用0.1mol•L-1盐酸滴定20mL 0.1mol•L-1氨水 | |
| B. | 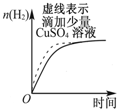 表示常温下,等量锌粉分别与两份足量的等体积等浓度的盐酸反应 | |
| C. | 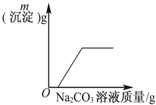 表示向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 | |
| D. |  表示向盐酸溶液中滴入氨水 |
13.已知两种弱酸的酸性:HA>HB,在常温下下列各项比较中正确的是( )
| A. | 两种溶液:①0.1mol/L HA溶液;②0.1mol/L HB溶液,分别与0.1mol/L NaOH溶液等体积混合后溶液中,c(H+):①<② | |
| B. | 等物质的量浓度的HA溶液与NaB溶液等体积的混合液:2c(Na+)═(A-)+c(B-)+c(HA)+c(HB) | |
| C. | pH=9的三种溶液①NaB;②NH3•H2O;③NaOH,由水电离出的c(OH-):①>②>③ | |
| D. | 物质的量浓度相等的NaA与NaB两溶液中:c(B-)>c(A-) |
12.酒精洒到桌面上起火后,用湿布立即扑盖的目的是( )
| A. | 降低温度 | B. | 隔约空气 | ||
| C. | 既降低温度又隔绝空气 | D. | 吸走洒出的酒精 |
9.观察以下物质的结构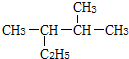 ,它的主链上含有( )个碳原子.
,它的主链上含有( )个碳原子.
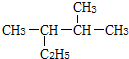 ,它的主链上含有( )个碳原子.
,它的主链上含有( )个碳原子.| A. | 四个 | B. | 五个 | C. | 六个 | D. | 七个 |
8.2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心,水是组成生命体的重要化学物质,有关水的反应很多.
(1)水分子自身作用会生成阴、阳两种离子,写出其电离方程式2H2O?H3O++OH-;现欲使水的电离平衡向右移动,且所得溶液显碱性,选择方法是BE.(填编号)
A.加入NaHSO4固体 B.加入Na2CO3固体 C.加热至100℃D.加入NH4C1固体 E.加入金属钠 F.通入氨气
(2)常温下,浓度均为0.1mo1•L-1的下列五种钠盐溶液pH如下表:
Na2CO3,Na2SO3溶液中,结合H+能力CO32->SO32-(填“大于”“等于”“小于”);根据表中数据,将等浓度的下列四种酸溶液分别稀释100倍,pH变化最大的是C(填编号).
A.HClO B.CH3COOH C.H2SO3 D.H2CO3.
0 172175 172183 172189 172193 172199 172201 172205 172211 172213 172219 172225 172229 172231 172235 172241 172243 172249 172253 172255 172259 172261 172265 172267 172269 172270 172271 172273 172274 172275 172277 172279 172283 172285 172289 172291 172295 172301 172303 172309 172313 172315 172319 172325 172331 172333 172339 172343 172345 172351 172355 172361 172369 203614
(1)水分子自身作用会生成阴、阳两种离子,写出其电离方程式2H2O?H3O++OH-;现欲使水的电离平衡向右移动,且所得溶液显碱性,选择方法是BE.(填编号)
A.加入NaHSO4固体 B.加入Na2CO3固体 C.加热至100℃D.加入NH4C1固体 E.加入金属钠 F.通入氨气
(2)常温下,浓度均为0.1mo1•L-1的下列五种钠盐溶液pH如下表:
| 溶质 | Na2CO3 | NaHCO3 | CH3COONa | Na2SO3 | NaHSO3 | NaClO |
| PH | 11.6 | 9.7 | 8.9 | 10.0 | 4.0 | 10.3 |
A.HClO B.CH3COOH C.H2SO3 D.H2CO3.
 乙苯
乙苯 2,3-二甲基戊烷
2,3-二甲基戊烷 3-甲基-1-丁烯
3-甲基-1-丁烯 .
.