9.下列关于化学的描述中,不正确的是( )
| A. | 化学是一门具有创造性和实用性的科学 | |
| B. | 人们可以利用先进的技术和设备在化学反应中制造出新原子和新分子 | |
| C. | 制陶、冶金及酿酒过程中,肯定发生了化学变化 | |
| D. | 化学家可以在微观层面上操纵分子和原子,组装分子器件和分子机器等 |
4. (1)如图是用于笔记本电脑的甲醇燃料电池结构示意图,a处充入的物质是甲醇(写名称),写出此电极的电极反应式CH3OH-6e-+H2O=CO2+6H+.
(1)如图是用于笔记本电脑的甲醇燃料电池结构示意图,a处充入的物质是甲醇(写名称),写出此电极的电极反应式CH3OH-6e-+H2O=CO2+6H+.
(2)若以该电池为电源,用石墨做电极电解200mL含有下列离子的溶液,
电解一段时间后,两极收集到相同体积(相同条件)的气体,(忽略溶液体积的变化及电极产物可能存在的溶解现象)则整个电解过程中阳极发生反应的电极反应式为2Cl --2e-=Cl2↑,4OH--4e-=2H2O+O2↑.
 (1)如图是用于笔记本电脑的甲醇燃料电池结构示意图,a处充入的物质是甲醇(写名称),写出此电极的电极反应式CH3OH-6e-+H2O=CO2+6H+.
(1)如图是用于笔记本电脑的甲醇燃料电池结构示意图,a处充入的物质是甲醇(写名称),写出此电极的电极反应式CH3OH-6e-+H2O=CO2+6H+.(2)若以该电池为电源,用石墨做电极电解200mL含有下列离子的溶液,
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 0.5 | 2 | 2 | 0.5 |
3.甲醇是一种可再生能源,具有开发和应用的广阔前景,研究甲醇具有重要意义.
(1)工业上可用C02和H2制取甲醇,已知下列反应的能量变化图:
则由二氧化碳和氢气制备甲醇的热化学方程式为CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H=-50KJ/mol.
(2)某化学研究性学习小组模拟用CO和H2合成甲醇,其反应为:CO(g)+2H2(g)
CH30H(g)△H<O.在容积固定为2L的密闭容器内充人1mol CO和2mol H2,加入合适的催化剂(体积可以忽略不计)、保持250℃不变发生上述反应,用压力计监测容器内压强的变化如下:
则反应从开始到20min时,以CO浓度变化表示的平均反应速率V(CO)=0.0125mol/(L•min),该温度下平衡常数K=4,若升高温度则K值减小(填增大、减小或不变).

(1)工业上可用C02和H2制取甲醇,已知下列反应的能量变化图:
则由二氧化碳和氢气制备甲醇的热化学方程式为CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H=-50KJ/mol.
(2)某化学研究性学习小组模拟用CO和H2合成甲醇,其反应为:CO(g)+2H2(g)
CH30H(g)△H<O.在容积固定为2L的密闭容器内充人1mol CO和2mol H2,加入合适的催化剂(体积可以忽略不计)、保持250℃不变发生上述反应,用压力计监测容器内压强的变化如下:
| 反应时间/min | O | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
2.下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A. | pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(OH-)相等 | |
| B. | 常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH) | |
| C. | 常温下物质的量浓度相等的①NH4HCO3、②NH4HSO4、③NH4Fe(SO4)2:三种溶液中NH4+的浓度:②>③>① | |
| D. | 等体积等物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数:N前>N后 |
1.下表中对应关系错误的是( )
0 172117 172125 172131 172135 172141 172143 172147 172153 172155 172161 172167 172171 172173 172177 172183 172185 172191 172195 172197 172201 172203 172207 172209 172211 172212 172213 172215 172216 172217 172219 172221 172225 172227 172231 172233 172237 172243 172245 172251 172255 172257 172261 172267 172273 172275 172281 172285 172287 172293 172297 172303 172311 203614
| A | NaCl═Na++Cl-; NH3•H2O?NH4++OH- | 均属于电离方程式 |
| B | Ba2++SO42-═BaSO4↓; HCO3-+OH-═CO32-+H2O | 均可表示一类反应 |
| C | 向溶液中滴加盐酸酸化过的BaCl2溶液,出现白色沉淀 | 说明该溶液中一定有SO42- |
| D | Cl2+2NaOH═NaCl+NaClO+H2O; 3S+6NaOH═2Na2S+Na2SO3+3H2O | Cl2和S在反应中既作氧化剂又作还原剂 |
| A. | A | B. | B | C. | C | D. | D |

 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$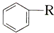 +HCl
+HCl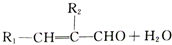
 .
. .
. .
. 氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题.
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题.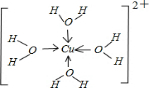 .
.
 和
和 .
.